Natriumion (Na+) vs. Neonatom (Ne):Nøgleforskelle forklaret
1. Antal elektroner:
* Natriumion (Na+): Har 10 elektroner. Den mister en elektron fra sin neutrale tilstand for at blive positivt ladet.
* Neonatom (Ne): Har 10 elektroner. Det er naturligt et neutralt atom, hvilket betyder, at det har det samme antal protoner og elektroner.
2. Opladning:
* Natriumion (Na+): Har en +1 ladning, fordi den mistede en elektron.
* Neonatom (Ne): Har en neutral ladning (0).
3. Elektronkonfiguration:
* Natriumion (Na+): 1s² 2s² 2p⁶ (samme som neon)
* Neonatom (Ne): 1s² 2s² 2p⁶
4. Kemisk reaktivitet:
* Natriumion (Na+): Er relativt ureaktiv på grund af dens stabile elektronkonfiguration.
* Neonatom (Ne): Er meget ureaktiv (en ædelgas) på grund af dens fulde ydre elektronskal.
I bund og grund har en natriumion den samme elektronkonfiguration som et neonatom, hvilket gør den meget stabil. Dette er grunden til, at natrium let mister sin ydre elektron for at danne en positiv ion.
Nøgleudtag: Natriumioner og neonatomer har forskellig kemisk adfærd på trods af at de har det samme antal elektroner og den samme elektronkonfiguration. Denne forskel skyldes det faktum, at natriumionen bærer en positiv ladning, mens neonatomet er neutralt.
 Varme artikler
Varme artikler
-
 Beregn mængden af overskydende reaktant:En trin-for-trin guideAf Claire Gillespie – Opdateret 30. august 2022 anyaivanova/iStock/GettyImages Den overskydende reaktant (også kaldet overskydende reagens) refererer til mængden af et kemikalie, der forbliver ureag
Beregn mængden af overskydende reaktant:En trin-for-trin guideAf Claire Gillespie – Opdateret 30. august 2022 anyaivanova/iStock/GettyImages Den overskydende reaktant (også kaldet overskydende reagens) refererer til mængden af et kemikalie, der forbliver ureag -
 Almindelig herbicidforbindelse kan redde millioner af livUQ -ph.d. -studerende Mario D. Garcia udfører et af de mange eksperimenter, der er involveret i forskningen. Kredit:University of Queensland En kemisk forbindelse, der findes i almindelige herbici
Almindelig herbicidforbindelse kan redde millioner af livUQ -ph.d. -studerende Mario D. Garcia udfører et af de mange eksperimenter, der er involveret i forskningen. Kredit:University of Queensland En kemisk forbindelse, der findes i almindelige herbici -
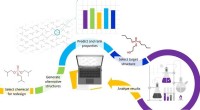 Sådan designes sikre og bæredygtige kemikalierMetode præsenteret af forskerne. Som et casestudie genererede de over seks millioner alternativer til en populær flammehæmmer og evaluerede deres egenskaber. Kredit:UvA/HIMS Med mange menneskeskabt
Sådan designes sikre og bæredygtige kemikalierMetode præsenteret af forskerne. Som et casestudie genererede de over seks millioner alternativer til en populær flammehæmmer og evaluerede deres egenskaber. Kredit:UvA/HIMS Med mange menneskeskabt -
 Udvikling af en måde at gøre oxygen injicerbarJarad Mason og hans team har skabt permanent porøst vand, hvilket gør det muligt at opbevare gasser i høje koncentrationer i væsken. Kredit:Kris Snibbe/Harvard Staff Photographer Hvad hvis akutmedi
Udvikling af en måde at gøre oxygen injicerbarJarad Mason og hans team har skabt permanent porøst vand, hvilket gør det muligt at opbevare gasser i høje koncentrationer i væsken. Kredit:Kris Snibbe/Harvard Staff Photographer Hvad hvis akutmedi
- Kunne det snart være spillet slut for Fortnite-dille?
- Bedste enhed til at måle afstand i nærheden af stjerner?
- Hvor mange millimeter er der i 7 centimeter?
- Europa har haft et koldt og vådt forår - men vil det vare hele sommeren?
- Forstå bakterier:Hvordan de formerer sig og spredes
- Hvad findes sukkeret i DNA?


