Beregn mængden af overskydende reaktant:En trin-for-trin guide
Af Claire Gillespie – Opdateret 30. august 2022
anyaivanova/iStock/GettyImages
Den overskydende reaktant (også kaldet overskydende reagens) refererer til mængden af et kemikalie, der forbliver ureageret, efter at en reaktion er nået til ende. Det bestemmes af det faktum, at den anden reaktant er blevet fuldstændig forbrugt og derfor ikke kan deltage yderligere. At kende den overskydende reaktant giver dig mulighed for at bestemme de endelige mængder af både produkt og resterende reaktant.
Ting påkrævet
- Periodisk tabel
- Lommeregner
1. Afbalancere reaktionen
Start med at afbalancere den kemiske ligning for at forstå de nøjagtige støkiometriske forhold, der kræves. Overvej f.eks. reaktionen:Mg(OH)2 + HCl → MgCl2 + H2 O. Den ubalancerede ligning viser en ubalance mellem brint-, klor- og oxygenatomer. Tilføjelse af en koefficient på 2 før HCl og 2 før H2 O afbalancerer ligningen:Mg(OH)2 + 2HCl → MgCl2 + 2H2 O.
2. Find molekylvægt
Konverter de givne masser af reaktanter til mol. Brug et periodisk system til at opnå atommasser:Mg = 24.305, O = 16.000, H = 1.008. For Mg(OH)2 , molekylvægten er 24.305 + (2 × 16.000) + (2 × 1.008) =58.305 g/mol.
3. Konverter masse til mol
Anvend formlen mol = gram ÷ molekylvægt . For 65 g Mg(OH)2 :65 ÷ 58,305 = 1,11 mol. For 57 g HCl (H = 1,008, Cl = 35,453):57 ÷ 36,461 = 1,56 mol.
4. Anvend den balancerede ligning
Brug de støkiometriske koefficienter fra den balancerede ligning. To mol HCl reagerer med et mol Mg(OH)2 . Beregn den begrænsende mængde:1,56 ÷ 2 = 0,78 mol HCl påkrævet. Siden 0,78 mol < 1,11 mol Mg(OH)2 , Mg(OH)2 er i overskud, og HCl er den begrænsende reaktant.
5. Bestem reaktantprocent og overskydende masse
Find brøkdelen af Mg(OH)2 der faktisk reagerede:0,78 ÷ 1,11 = 0,704 (70,4 %). Multiplicer den oprindelige masse af Mg(OH)2 ved denne brøk for at opnå den anvendte mængde:65 × 0,704 = 45,78 g. Træk dette fra startmassen for at finde overskuddet:65 – 45,78 = 19,21 g Mg(OH)2 forblive ureageret.
 Varme artikler
Varme artikler
-
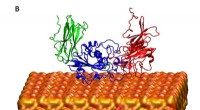 XSEDE-supercomputertildelinger på Stampede1 og Comet hjælper med at prøve proteinfoldning i knogl…XSEDE-supercomputere Stampede ved TACC og Comet ved SDSC hjalp studieforfattere med at simulere hovedstykkedomænet af cellemembranproteinreceptorintegrinet i opløsning, baseret på molekylær dynamik mo
XSEDE-supercomputertildelinger på Stampede1 og Comet hjælper med at prøve proteinfoldning i knogl…XSEDE-supercomputere Stampede ved TACC og Comet ved SDSC hjalp studieforfattere med at simulere hovedstykkedomænet af cellemembranproteinreceptorintegrinet i opløsning, baseret på molekylær dynamik mo -
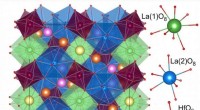 Forskere syntetiserer et nyt fosforKrystallstruktur af forbindelsen. Kredit:Yana Baklanova (medforfatter af undersøgelsen) Kemikere og fysikere fra Ural Federal University og Institute of Chemistry of Faststoffer fra Ural Branch of
Forskere syntetiserer et nyt fosforKrystallstruktur af forbindelsen. Kredit:Yana Baklanova (medforfatter af undersøgelsen) Kemikere og fysikere fra Ural Federal University og Institute of Chemistry of Faststoffer fra Ural Branch of -
 Hvordan vand hjælper substratet ind i enzymetKredit:Pixabay/CC0 Public Domain Forskere fra Bochum og Berkeley har undersøgt, hvorfor bure kan øge den katalytiske aktivitet af lukkede molekyler. Ved at bruge terahertz-spektroskopi og kompleks
Hvordan vand hjælper substratet ind i enzymetKredit:Pixabay/CC0 Public Domain Forskere fra Bochum og Berkeley har undersøgt, hvorfor bure kan øge den katalytiske aktivitet af lukkede molekyler. Ved at bruge terahertz-spektroskopi og kompleks -
 De kemiske hemmeligheder bag vanilje lokkerKredit:CC0 Public Domain Fra is til lattes er vanilje et af de mest populære krydderier i verden. Det er også en af de mest arbejdskrævende at producere, og genveje fører til et mindre velsmagend
De kemiske hemmeligheder bag vanilje lokkerKredit:CC0 Public Domain Fra is til lattes er vanilje et af de mest populære krydderier i verden. Det er også en af de mest arbejdskrævende at producere, og genveje fører til et mindre velsmagend
- Hvad er virkningen på miljøet på grund af ikke -konventionel energi?
- Eksempler på indikatorarter
- Bedre visning gennem fluorescerende nanorør, når du kigger ind i en mus
- Hvorfor indeholder et vandmolekyle to atomer, men kun hydrogencholrid?
- Hvornår er latter et medicinsk symptom?
- Hvordan maskingeværet revolutionerede krigsførelse


