At skrive kemiske formler for overgangsmetalforbindelser – en trin-for-trin guide
artisteer/iStock/GettyImages
Skrivning af kemiske formler for overgangsmetalforbindelser – en trin-for-trin guide
Overgangsmetaller, som optager gruppe 3-12 i det periodiske system, kan danne ioner med flere ladninger, fordi de mister forskellige antal elektroner. Navnet på en forbindelse fortæller dig, hvilken ladning der er til stede, enten med et romertal i det moderne IUPAC-system eller ved de traditionelle "ic"/"ous" suffikser.
Moderne (romertal) vs. traditionel (ic/ous) navngivning
- romertal angiv den nøjagtige oxidationstilstand, der anvendes i forbindelsen (f.eks. jern(III)chlorid =Fe 3+ Cl −1 ).
- ic/ous suffikser beskriv almindelige oxidationstilstande:"ic" for den mest almindelige positive ladning og "ous" for en mindre (f.eks. jern =Fe 3+ , jernholdig =Fe 2+ ).
Trin-for-trin metode til at skrive formlen
- Identificer de elementære symboler. Brug om nødvendigt det periodiske system. For polyatomiske anioner skal du omslutte hele gruppen i parentes (f.eks. SO4 2− ).
- Tildel ioniske ladninger. Skriv hver ions ladning som et overskrift ved siden af dens symbol for at hjælpe med at balancere. Disse hævet skrift er kun et mellemtrin og vises ikke i den endelige formel.
- Eksempel:jern(III)chlorid → Fe 3+ Cl −1 (Fe 3+ Cl −1 ).
- Eksempel:jern(III)sulfat → Fe 3+ (SO4 ) 2− .
- Balancer afgifterne. Konverter de hævede skrifter til sænkede, så den samlede afgift er lig med nul.
- For FeCl3 :en Fe 3+ balancerer med tre Cl −1 .
- For Fe2 (SO4 )3 :to Fe 3+ balance med tre SO4 2− .
Illustrativt eksempel
Hvad er formlen for kobber(II)oxid?
- Ordet "cuprous" angiver Cu +1 .
- Oxygen er altid O −2 .
- Afbalancering af afgifterne giver Cu2 O.
Ved at følge disse trin kan du trygt skrive nøjagtige kemiske formler for enhver overgangsmetalforbindelse.
 Varme artikler
Varme artikler
-
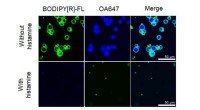 Syntetiserer kemisk-sansende celler fra bundenEn undersøgelse offentliggjort i Journal of the America n Chemical Society, syntetiserede kunstige celler for at påvise histamin. Da histamin blev påvist, udtrykte de kunstige celler et enzym, der for
Syntetiserer kemisk-sansende celler fra bundenEn undersøgelse offentliggjort i Journal of the America n Chemical Society, syntetiserede kunstige celler for at påvise histamin. Da histamin blev påvist, udtrykte de kunstige celler et enzym, der for -
 Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s
Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s -
 Ny opdagelse af plutonium viser vejen til at rense atomaffaldThomas Albrecht-Schmitt er Gregory R. Choppin professor i kemi ved Florida State University. Kredit:Bill Lax/Florida State University Plutonium har længe været en del af mange landes atomenergistr
Ny opdagelse af plutonium viser vejen til at rense atomaffaldThomas Albrecht-Schmitt er Gregory R. Choppin professor i kemi ved Florida State University. Kredit:Bill Lax/Florida State University Plutonium har længe været en del af mange landes atomenergistr -
 Minimering af brændstofeksplosioner og brande fra ulykker og terrorhandlinger med polymererNye polymerbrændstofadditiver er bedre til at reducere eksplosive brande (nederst) end konventionelle additiver (øverst). Kredit:Julia Kornfield Når en terrorhandling eller et køretøj eller en ind
Minimering af brændstofeksplosioner og brande fra ulykker og terrorhandlinger med polymererNye polymerbrændstofadditiver er bedre til at reducere eksplosive brande (nederst) end konventionelle additiver (øverst). Kredit:Julia Kornfield Når en terrorhandling eller et køretøj eller en ind
- Hvilken klassificering af fluor?
- Nyt papir viser, hvordan sygdomme kan påvirke økonomier i generationer
- Hvad er den typiske størrelse af hvid dværg i solradier?
- Hvad er en metode til kulekstraktion, der bruger store stykker jordbevægelsesudstyr til at fjerne e…
- Hvorfor studerer astronomer nebler?
- Ksp og ionprodukt:Bestemmelse af opløsningsmætning


