Ionisering af ikke-metaller:Forståelse af aniondannelse
* Ikke-metaller har en høj elektronegativitet: Det betyder, at de har en stærk tiltrækning af elektroner.
* De har en tendens til at være tættere på en hel oktet: Ikke-metaller har typisk et større antal valenselektroner (elektroner i den yderste skal) sammenlignet med metaller. Ved at få elektroner kan de opnå en stabil elektronkonfiguration, der ligner den nærmeste ædelgas.
Her er en oversigt:
1. Elektronforstærkning: Et ikke-metalatom får en eller flere elektroner fra et andet atom.
2. Danning af anion: Atomet bliver negativt ladet, da det nu har flere elektroner end protoner.
3. Stabil elektronkonfiguration: Anionen opnår en stabil elektronkonfiguration, der ligner en ædelgas.
Eksempel:
* Klor (Cl), et ikke-metal, har 7 valenselektroner.
* Når den får én elektron, bliver den til en chloridion (Cl⁻).
* Cl⁻ har nu 8 valenselektroner, svarende til den stabile elektronkonfiguration af argon (Ar).
Vigtige bemærkninger:
* Antallet af opnåede elektroner afhænger af det specifikke ikke-metal. For eksempel får oxygen (O) to elektroner til at danne oxidionen (O²⁻).
* Ioniseringsprocessen ledsages ofte af dannelsen af ioniske forbindelser. Dette sker, når et metalatom mister elektroner (danner en kation), og et ikke-metalatom får elektroner (danner en anion), hvilket resulterer i elektrostatisk tiltrækning mellem dem.
Sig til, hvis du har andre spørgsmål!
 Varme artikler
Varme artikler
-
 Antistof mod kræftfremkaldende stof dechifreretNår fedt reagerer med glødende kul ved en grill, der dannes et stof, som kemikerne kalder benzopyren. Det er et udbredt miljøgift, der kan forårsage kræft hos mennesker. Kredit:Fotolia/Dederer Som
Antistof mod kræftfremkaldende stof dechifreretNår fedt reagerer med glødende kul ved en grill, der dannes et stof, som kemikerne kalder benzopyren. Det er et udbredt miljøgift, der kan forårsage kræft hos mennesker. Kredit:Fotolia/Dederer Som -
 En ny udsigt til brillerKredit:CC0 Public Domain Forskere ved University of Tokyo introducerede en ny fysisk model, der forudsiger dynamikken i glasagtige materialer udelukkende baseret på deres lokale grad af atomstrukt
En ny udsigt til brillerKredit:CC0 Public Domain Forskere ved University of Tokyo introducerede en ny fysisk model, der forudsiger dynamikken i glasagtige materialer udelukkende baseret på deres lokale grad af atomstrukt -
 Nye muligheder for lysemitterende plast med mønstret lysMønstret lys i form af en fisk. Kredit:Mattias Lindh Lysemitterende plast bruges i dag i tv- og smartphone-skærme, lysemitterende indikatorer og som belysning til biler og fly med særlige krav. Vi
Nye muligheder for lysemitterende plast med mønstret lysMønstret lys i form af en fisk. Kredit:Mattias Lindh Lysemitterende plast bruges i dag i tv- og smartphone-skærme, lysemitterende indikatorer og som belysning til biler og fly med særlige krav. Vi -
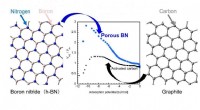 Fange gasser bedre med bornitrid-nanoporerSkematisk illustration af bornitrid- og kulstofstrukturer og adsorptionsevne på porøse bornitrid- og kulstofmaterialer. Kredit:2021 Takahiro Ohkubo Hvad er fælles mellem en teknologi til lagring a
Fange gasser bedre med bornitrid-nanoporerSkematisk illustration af bornitrid- og kulstofstrukturer og adsorptionsevne på porøse bornitrid- og kulstofmaterialer. Kredit:2021 Takahiro Ohkubo Hvad er fælles mellem en teknologi til lagring a


