Argonbinding:Kovalent vs. ionisk - Forståelse af ædelgasadfærd
Derfor argon danner ikke kovalente eller ioniske bindinger.
Her er hvorfor:
* Kovalente bindinger involverer deling af elektroner mellem atomer. Argon har en fuld ydre skal af elektroner, hvilket gør det meget stabilt og ikke-reaktivt. Det behøver ikke at dele elektroner for at opnå stabilitet.
* ioniske bindinger involverer overførsel af elektroner mellem atomer, hvilket resulterer i positivt og negativt ladede ioner, der tiltrækker hinanden. Argons stabile elektronkonfiguration gør det usandsynligt, at det taber eller får elektroner til at danne ioner.
Sammenfattende forhindrer argons manglende reaktivitet og stabile elektronkonfiguration det i at danne nogen form for kemiske bindinger.
 Varme artikler
Varme artikler
-
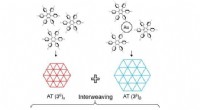 Meget kompleks todimensionel tessellation i den molekylære verdenFigur viser tre typer af meget komplekse sammenvævede tesselleringer baseret på to forskellige molekylære faser konstrueret af en enkelt molekylær byggesten. Kredit:Nature Communications Tessellat
Meget kompleks todimensionel tessellation i den molekylære verdenFigur viser tre typer af meget komplekse sammenvævede tesselleringer baseret på to forskellige molekylære faser konstrueret af en enkelt molekylær byggesten. Kredit:Nature Communications Tessellat -
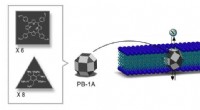 Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to
Syntetiske nanokanaler til jodidtransport3-D struktur af den syntetiske iodid-transporter PB-1A udviklet af IBS forskere. PB-1A-design følger formen af 26-sidet polyeder lavet af trekanter og firkanter (mørkegrå) med 12 flader efterladt to -
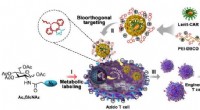 Forskere udvikler kunstige kemiske receptorer til at hjælpe viral transduktion til T-celleteknikAnvendelse af kunstig kemisk receptor i CAR-konstrueret T-cellefremstilling og immunterapi af tumor. Kredit:CAI Lintao Konstrueret T-celle immunterapi, såsom kimærisk antigenreceptor T-celle (CAR-
Forskere udvikler kunstige kemiske receptorer til at hjælpe viral transduktion til T-celleteknikAnvendelse af kunstig kemisk receptor i CAR-konstrueret T-cellefremstilling og immunterapi af tumor. Kredit:CAI Lintao Konstrueret T-celle immunterapi, såsom kimærisk antigenreceptor T-celle (CAR- -
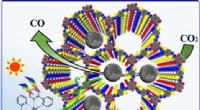 Ny undersøgelse belyser design af heterogene katalysatorer til selektiv kuldioxidfotoreduktionKredit:WANG Ruihus gruppe Anvendelse af kovalente organiske rammer (COFer) som heterogene katalysatorer for fotokatalytisk CO 2 reduktion har tiltrukket sig betydelig opmærksomhed på grund af de
Ny undersøgelse belyser design af heterogene katalysatorer til selektiv kuldioxidfotoreduktionKredit:WANG Ruihus gruppe Anvendelse af kovalente organiske rammer (COFer) som heterogene katalysatorer for fotokatalytisk CO 2 reduktion har tiltrukket sig betydelig opmærksomhed på grund af de
- Skelsættende undersøgelse finder, at håndtering af ulighed er nøglen til at realisere FN's mål
- Hvad er vinkelhastigheden i radianer pr. Sekund af et hjul, der roterer ved O 18 o / min?
- Brunt Ice Shelf i Antarktis kælver nyt isbjerg
- Nyopdagede supernova-rester afslører kun sig selv ved de højeste gammastråleenergier
- Hvilke reaktanter bruges under fotosyntesen?
- Er der en nulfysikteori?


