Elektrondomæne for NO2:En trin-for-trin guide
1. Tegn Lewis-strukturen
* Nitrogen (N) er det centrale atom, og det har 5 valenselektroner.
* Ilt (O) har hver 6 valenselektroner.
Lewis-strukturen ser sådan ud:
O
||
N - O
2. Tæl elektrondomænerne
Et elektrondomæne er et område i rummet omkring et atom, hvor elektroner er koncentreret. Det kan være en enkeltbinding, en dobbeltbinding, en tredobbeltbinding eller et ensomt elektronpar.
* I NO2 er der tre elektrondomæner omkring det centrale nitrogenatom:
* Én dobbeltbinding til venstre oxygenatom.
* Én dobbeltbinding til det højre iltatom.
* Et ensomt elektronpar på nitrogenatomet.
3. Bestem elektrondomæne-geometrien
Baseret på de tre elektrondomæner er elektrondomænets geometri trigonal plan . Det betyder, at elektrondomænerne er arrangeret i en trekantet form omkring nitrogenatomet.
Vigtig bemærkning: Mens elektrondomæne-geometrien er trigonal plan, er den *molekylære* geometri af NO2 bøjet på grund af tilstedeværelsen af det enlige par på nitrogenatomet. Enlige par udøver en større frastødende kraft på bindingsparrene, hvilket får molekylet til at bøje.
 Varme artikler
Varme artikler
-
 Rens gennem solenergiDemonstrator for en mobil målepistol med selvlysende polymerbærer. Kredit:Fraunhofer IST / Falko Oldenburg I kombination med de rigtige materialer, solstråler kan gøre underværker:de renser bygnin
Rens gennem solenergiDemonstrator for en mobil målepistol med selvlysende polymerbærer. Kredit:Fraunhofer IST / Falko Oldenburg I kombination med de rigtige materialer, solstråler kan gøre underværker:de renser bygnin -
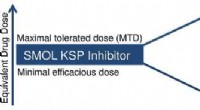 Fleksibel, stabil og potent mod kræft - ny tilgang til tumorbehandlingKredit:Angewandte Chemie At koble terapeutisk aktive molekyler til specifikke antistoffer kan hjælpe med at pilotere dem til deres udpegede mål og minimere bivirkninger - især ved behandling af tu
Fleksibel, stabil og potent mod kræft - ny tilgang til tumorbehandlingKredit:Angewandte Chemie At koble terapeutisk aktive molekyler til specifikke antistoffer kan hjælpe med at pilotere dem til deres udpegede mål og minimere bivirkninger - især ved behandling af tu -
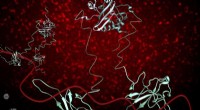 Dybt dyk ned i vigtige COVID-19-proteiner er et skridt mod nye lægemidler, vaccinerNukleocapsid-phosphoproteinet (blåt) af SARS-CoV-2 (N) (grå) spiller kritiske roller i flere processer i SARS-CoV-2-infektionscyklussen, inklusive replikation og transskription, og pakning og beskytte
Dybt dyk ned i vigtige COVID-19-proteiner er et skridt mod nye lægemidler, vaccinerNukleocapsid-phosphoproteinet (blåt) af SARS-CoV-2 (N) (grå) spiller kritiske roller i flere processer i SARS-CoV-2-infektionscyklussen, inklusive replikation og transskription, og pakning og beskytte -
 En farverig detektorKredit:Pixabay/CC0 Public Domain Forskere ved University of Tsukuba har udviklet en ny slags farveskiftende krystallinsk materiale, der kan bruges til at indikere tilstedeværelsen af vand. Ændri
En farverig detektorKredit:Pixabay/CC0 Public Domain Forskere ved University of Tsukuba har udviklet en ny slags farveskiftende krystallinsk materiale, der kan bruges til at indikere tilstedeværelsen af vand. Ændri
- To planeter, der kredser om Teegardens-stjernen, er beskrevet som mest jordlignende fundet endnu
- Energien i varme kaldes også?
- Lov, der giver størrelserne på kredsløbsplaneter, betragtes ikke længere som en fysisk, fordi de…
- Hvorfor er teksturer og vægt forskellige fra kalksten marmor?
- Hvilke resultater på Jorden, når solen og månen er på linje?
- Hvordan bliver jeg astronaut?


