Kobberkorrosion og pH:en hypotese om vands surhed
Hypotese:
Hastigheden af kobberkorrosion vil stige, når pH-værdien af vandet falder (bliver surere).
Forklaring:
Kobberkorrosion er primært drevet af elektrokemiske reaktioner, hvor kobberatomer mister elektroner og bliver oxideret. Denne proces er påvirket af tilstedeværelsen af opløst oxygen og hydrogenioner (H+) i vandet.
* Sure miljøer (lav pH): Højere koncentrationer af H+ ioner i surt vand forstærker de elektrokemiske reaktioner ved at give en større drivkraft for kobberoxidation. Dette fører til en hurtigere korrosionshastighed.
* Alkaliske miljøer (høj pH): Under alkaliske forhold kan tilstedeværelsen af hydroxidioner (OH-) danne et beskyttende oxidlag på kobberoverfladen, hvilket hæmmer korrosion.
Derfor vil et fald i pH resultere i en højere koncentration af H+ ioner, hvilket accelererer de elektrokemiske reaktioner og fører til øget kobberkorrosion.
Bemærk: Dette er en generel hypotese, og det faktiske forhold mellem pH og kobberkorrosion kan være komplekst og påvirket af andre faktorer som temperatur, opløste salte og tilstedeværelsen af andre metaller.
Sidste artikelAtomer i et mol metan (CH4):En detaljeret beregning
Næste artikelBariumchlorid og forbrænding:Forståelse af kemiske reaktioner
 Varme artikler
Varme artikler
-
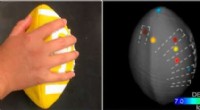 Robotics tager massespecifikationer til den tredje dimension for retsmedicin, farma applikationerVed at kombinere en robotarm og massespektrometri, forskere kan analysere overfladen af 3D-objekter, såsom fodbolde. Kredit:American Chemical Society Inden for det seneste årti, der er gjort man
Robotics tager massespecifikationer til den tredje dimension for retsmedicin, farma applikationerVed at kombinere en robotarm og massespektrometri, forskere kan analysere overfladen af 3D-objekter, såsom fodbolde. Kredit:American Chemical Society Inden for det seneste årti, der er gjort man -
 Ny proces til fuld udnyttelse af nåletræsbark klar til produktionKredit:Adobe Stock Papirmasse- og papirindustrien og træproduktindustrien i Finland producerer tilsammen tre millioner tons bark af nåletræ som affald hvert år. Det meste af dette bruges i energip
Ny proces til fuld udnyttelse af nåletræsbark klar til produktionKredit:Adobe Stock Papirmasse- og papirindustrien og træproduktindustrien i Finland producerer tilsammen tre millioner tons bark af nåletræ som affald hvert år. Det meste af dette bruges i energip -
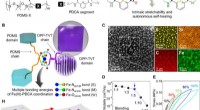 Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter
Strækbar, selvhelbredende og halvledende polymerfilm til elektronisk hud (e-skin)Design og karakterisering af belastningsfølsomme, strækbar, og selvhelbredende halvledende film. (A) Kemisk struktur af DPP halvledende polymer, PDMS, og PDCA-del introduceret i begge polymerskeletter -
 Store molekyler fra kostfibre kan ændre tarmmiljøet gennem fysiske kræfterKredit:CC0 Public Domain Store molekyler fra kostfibre, kaldet polymerer, kan fysisk påvirke miljøet i tyndtarmen ved at få faste partikler til at gruppere sig (eller aggregere), ifølge forskning
Store molekyler fra kostfibre kan ændre tarmmiljøet gennem fysiske kræfterKredit:CC0 Public Domain Store molekyler fra kostfibre, kaldet polymerer, kan fysisk påvirke miljøet i tyndtarmen ved at få faste partikler til at gruppere sig (eller aggregere), ifølge forskning
- Hvad måles energi på?
- Hvordan man fortæller, om en egern er Mand eller Kvinde
- Mestring af fremtidens elnet
- Hvordan adskiller du et uopløseligt fast stof fra et opløseligt fast stof.?
- Omfanget af forskelsbehandling i disciplinen af studerende med handicap uklart
- Hvad er de vigtigste træk ved mantel?


