Bariumchlorid og forbrænding:Forståelse af kemiske reaktioner
Her er hvorfor:
* Det er et salt: Bariumchlorid er en ionisk forbindelse, ikke et brændbart materiale som træ eller brændstof. Det har ikke den kemiske struktur til at undergå forbrænding.
* Ingen oxidationsreaktion: Forbrænding kræver en hurtig reaktion med ilt (oxidation), der frigiver varme og lys. Bariumchlorid reagerer ikke med ilt på denne måde.
Selvom bariumchlorid i sig selv ikke brænder, kan det bruges til at producere en grøn flamme i fyrværkeri. Dette skyldes, at bariumionerne i forbindelsen udsender grønt lys, når de opvarmes til en høj temperatur.
Det er dog vigtigt at bemærke, at håndtering af bariumchlorid kræver forsigtighed da det er giftigt.
Sidste artikelKobberkorrosion og pH:en hypotese om vands surhed
Næste artikelVandfri citronsyreformel:C6H8O7 Forklaret
 Varme artikler
Varme artikler
-
 Kemikere bygger naturlig anti-cancer forbindelse med en effektiv ny procesKredit:CC0 Public Domain Scripps Research kemikere Hans Renata, Ph.D., og Alexander Adibekian, Ph.D., har opdaget en måde til effektivt at skabe en syntetisk version af en værdifuld naturlig forbi
Kemikere bygger naturlig anti-cancer forbindelse med en effektiv ny procesKredit:CC0 Public Domain Scripps Research kemikere Hans Renata, Ph.D., og Alexander Adibekian, Ph.D., har opdaget en måde til effektivt at skabe en syntetisk version af en værdifuld naturlig forbi -
 Forskere forbedrer et fotosyntetisk enzym ved at tilføje fluoroforerUdvidelse af enzymets bånd af lysbølgelængder, der kan høstes, er en vigtig forbedring i betragtning af sollysets ekstremt lave energitæthed. Kredit:Takehisa Dewa fra Nagoya Institute of Technology
Forskere forbedrer et fotosyntetisk enzym ved at tilføje fluoroforerUdvidelse af enzymets bånd af lysbølgelængder, der kan høstes, er en vigtig forbedring i betragtning af sollysets ekstremt lave energitæthed. Kredit:Takehisa Dewa fra Nagoya Institute of Technology -
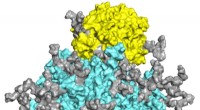 Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit
Ofte overset, molekyler kaldet glykaner regulerer COVID-19-spidsproteinfunktionenEn molekylær model viser det stærkt glykosylerede SARS-CoV-2-spidsprotein (cyan, med glykaner i grå og andre farver) bundet til den cellulære ACE2-receptor (gul). En ny undersøgelse fremhæver den krit -
 Uigennemsigtigt plast:definition, nøgletyper og industrielle anvendelserAf Clare Edwards, Opdateret 24. marts 2022 Uigennemsigtig plast er materialer, der blokerer for alt lys, og gør dem fuldstændig ugennemsigtige. Nogle polymerer udviser naturligt denne egenskab på gru
Uigennemsigtigt plast:definition, nøgletyper og industrielle anvendelserAf Clare Edwards, Opdateret 24. marts 2022 Uigennemsigtig plast er materialer, der blokerer for alt lys, og gør dem fuldstændig ugennemsigtige. Nogle polymerer udviser naturligt denne egenskab på gru
- Hvilken effekt har friktion på hastigheden af et bevægende objekt?
- Hvad er accelerationsafgiften til tyngdekraften nær jordoverfladen?
- Ny Pompeji-fund fremhæver middelklasselivet i dødsdømt by
- Hvordan krop producerer varme?
- Vi skal tale:Kommunikation forhindrer passivitet ved at udnytte goodwill
- Hvad betyder ikke Energy Star -kompatible?


