Svag syre + stærk syrereaktion:Forståelse af kemien
* Stærke syrer dissocierer fuldstændigt i opløsning: Stærke syrer, som saltsyre (HCl) eller svovlsyre (H₂SO4), ioniseres fuldstændigt i vand og frigiver deres hydrogenioner (H⁺) og anioner.
* Svage syrer dissocierer delvist: Svage syrer, som eddikesyre (CH₃COOH) eller kulsyre (H₂CO₃), ioniseres kun delvist i vand. De eksisterer i ligevægt mellem den udissocierede syreform og de dissocierede ioner.
* Equilibrium Shift: Den høje koncentration af H⁺-ioner fra den stærke syre vil skubbe ligevægten af den svage syrereaktion til venstre, hvilket favoriserer den udissocierede form af den svage syre. Det betyder, at den svage syre ikke vil reagere væsentligt med den stærke syre.
I det væsentlige dominerer den stærke syre opløsningen og undertrykker ioniseringen af den svage syre. Der sker ingen nævneværdig kemisk ændring.
Eksempel:
Hvis du blander eddikesyre (CH₃COOH, en svag syre) med saltsyre (HCl, en stærk syre), vil HCl'en dissociere fuldstændigt til H⁺- og Cl⁻-ioner. H⁺-ionerne fra HCl vil undertrykke ioniseringen af eddikesyren, hvilket forhindrer den i at donere sine H⁺-ioner. Opløsningen forbliver sur med en høj koncentration af H⁺-ioner primært fra HCl.
Vigtig bemærkning: Selvom der ikke forekommer nogen signifikant reaktion, kan tilsætning af en svag syre til en stærk syreopløsning påvirke pH. Den svage syre kan fungere som en buffer, der hjælper med at modstå ændringer i pH, når mere stærk syre tilsættes.
 Varme artikler
Varme artikler
-
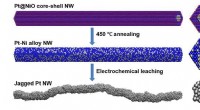 Ru overflader giver yderligere steder for energigenererende reaktioner i brændselscellerFlere aktive steder og mere overfladeareal på katalysatorer fremskynder den kemiske omdannelse af ilt og brint til vand og elektroner, generere elektricitet. Forskere udtænkte en ny synteserute for at
Ru overflader giver yderligere steder for energigenererende reaktioner i brændselscellerFlere aktive steder og mere overfladeareal på katalysatorer fremskynder den kemiske omdannelse af ilt og brint til vand og elektroner, generere elektricitet. Forskere udtænkte en ny synteserute for at -
 Transformering af kuldioxid – forskere udvikler ny to-trins CO2-konverteringsteknologiUD Professor Feng Jiaos team konstruerede en elektrolysator, afbilledet her, at gennemføre deres nye to-trins konverteringsproces. Kredit:Feng Jiao Et team af forskere ved University of Delawares
Transformering af kuldioxid – forskere udvikler ny to-trins CO2-konverteringsteknologiUD Professor Feng Jiaos team konstruerede en elektrolysator, afbilledet her, at gennemføre deres nye to-trins konverteringsproces. Kredit:Feng Jiao Et team af forskere ved University of Delawares -
 Flappende vinger drevet af solenDenne lille fløj kunne en dag bruges i robotter eller enheder til at høste solenergi. Kredit:American Chemical Society I oldgræsk mytologi, Icarus voksvinger smeltede, da han turde flyve for tæt p
Flappende vinger drevet af solenDenne lille fløj kunne en dag bruges i robotter eller enheder til at høste solenergi. Kredit:American Chemical Society I oldgræsk mytologi, Icarus voksvinger smeltede, da han turde flyve for tæt p -
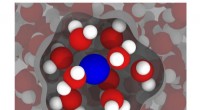 Moderne simuleringer kan forbedre MRI'erEn illustration baseret på simuleringer fra Rice Universitys ingeniører viser en gadoliniumion (blå) i vand (rød og hvid), med vand i den indre sfære - det vand, der er mest påvirket af gadolinium - f
Moderne simuleringer kan forbedre MRI'erEn illustration baseret på simuleringer fra Rice Universitys ingeniører viser en gadoliniumion (blå) i vand (rød og hvid), med vand i den indre sfære - det vand, der er mest påvirket af gadolinium - f


