Forstå bufferløsninger:Opretholdelse af pH-stabilitet
Her er hvorfor bufferløsninger virker:
* Komposition: Bufferopløsninger indeholder en svag syre og dens konjugerede base (eller en svag base og dens konjugerede syre).
* Ligevægt: Den svage syre og dens konjugerede base eksisterer i ligevægt. Det betyder, at de kan reagere med tilsatte syrer eller baser for at neutralisere dem.
* Neutralisering:
* Når en stærk syre tilsættes, reagerer konjugatbasen i bufferen med syren og danner den svage syre og vand. Dette minimerer faldet i pH.
* Når en stærk base tilsættes, reagerer den svage syre i bufferen med basen og danner den konjugerede base og vand. Dette minimerer stigningen i pH.
Eksempel:
En almindelig bufferopløsning fremstilles af eddikesyre (CH3COOH) og dens konjugerede base, acetation (CH3COO⁻).
* Når en stærk syre tilsættes, reagerer acetationen med syren og danner eddikesyre, hvilket forhindrer et stort fald i pH.
* Når en stærk base tilsættes, reagerer eddikesyren med basen og danner acetation, hvilket forhindrer en stor stigning i pH.
Vigtigheden af bufferløsninger:
Bufferopløsninger er utrolig vigtige i mange biologiske og kemiske systemer:
* Biologiske systemer: Buffere hjælper med at opretholde pH i blod, celler og andre biologiske væsker inden for snævre områder, der er afgørende for livet.
* Kemiske reaktioner: Bufferopløsninger bruges i kemiske reaktioner for at sikre, at pH-værdien forbliver konstant, hvilket kan være afgørende for, at reaktionen kan forløbe effektivt.
* Laboratorieforskning: Buffere bruges i vid udstrækning i laboratorieforsøg til at kontrollere opløsningernes pH.
Lad mig vide, hvis du gerne vil vide mere om specifikke typer bufferløsninger, eller hvordan de bruges i bestemte applikationer!
Sidste artikelJernoxider:formler, typer og egenskaber
Næste artikelForstå dobbeltbindingen mellem iltatomer
 Varme artikler
Varme artikler
-
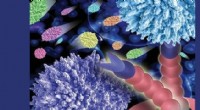 Multisample teknik til at analysere celleadhæsionDet nye assay, der er udviklet hos KAUST, er et fluorescerende multipleks celle-rullende assay, der bruger unikke fluorescerende tags til at mærke op til syv cellepopulationstyper. Kredit:© 2020 Elham
Multisample teknik til at analysere celleadhæsionDet nye assay, der er udviklet hos KAUST, er et fluorescerende multipleks celle-rullende assay, der bruger unikke fluorescerende tags til at mærke op til syv cellepopulationstyper. Kredit:© 2020 Elham -
 Turende strukturer i et menneskeskabt interfaceReaktionsdiffusionsprocessen drev dannelsen af den komplicerede uorganiske Turing -struktur. Kredit:ZHANG Xiaolong I 1952, Alan Turing, far til datalogi og kunstig intelligens, foreslået, at vis
Turende strukturer i et menneskeskabt interfaceReaktionsdiffusionsprocessen drev dannelsen af den komplicerede uorganiske Turing -struktur. Kredit:ZHANG Xiaolong I 1952, Alan Turing, far til datalogi og kunstig intelligens, foreslået, at vis -
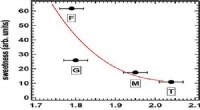 Vand kan være nøglen til at forstå sødmeKredit:American Chemical Society Et tranebær, honning eller en slikbar - hvad smager sødest? Disse fødevarer indeholder sukkerarter, som mennesker kan opfatte forskelligt. Et tranebær virker syrli
Vand kan være nøglen til at forstå sødmeKredit:American Chemical Society Et tranebær, honning eller en slikbar - hvad smager sødest? Disse fødevarer indeholder sukkerarter, som mennesker kan opfatte forskelligt. Et tranebær virker syrli -
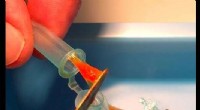 Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky
Sneglelim afslører ledetråde til at lave bedre medicinske klæbemidlerForskere studerer, hvordan sneglelim opnår sin stærke klæbeevne og fleksibilitet, indsigt, der kunne bruges til at skabe bedre medicinske klæbemidler. Kredit:Rebecca Falconer, Ithaca College Dusky
- Fundet på kromosomer bestemmer de specifikke egenskaber ved organismen?
- Hvad får slim til at vokse i mørk videnskabelig forklaring?
- Hvad skal du vide om næste uges totale solformørkelse i USA, Mexico og Canada
- Sprækkede iskapper på Mars
- I hvilken proces bruger cellen en vesikel til at flytte molekyler til celle?
- Hvordan skriver du den afbalancerede ligning mellem en syre og en base?


