Krystaldannelse:Forståelse af ionisk tiltrækning og energiminimering
1. Elektrostatisk tiltrækning:
* Ioner er atomer, der har fået eller mistet elektroner, hvilket giver dem en netto positiv eller negativ ladning.
* Modsatte ladninger tiltrækker, så positive og negative ioner trækkes til hinanden.
* Denne stærke elektrostatiske tiltrækning er det, der holder ionerne sammen.
2. Minimering af energi:
* Ioner ønsker naturligt at nå en tilstand med lavere energi.
* Krystaldannelse gør det muligt for ioner at opnå denne lavenergitilstand ved at arrangere sig selv i en højordnet, tredimensionel gitterstruktur.
* I dette gitter er hver ion omgivet af ioner med den modsatte ladning, hvilket maksimerer elektrostatisk tiltrækning og minimerer frastødning.
3. Processen:
* Kernedannelse: Små klynger af ioner begynder at dannes, når de samles i en opløsning eller smelter.
* Vækst: Flere ioner binder sig til disse klynger, hvilket fører til dannelsen af større og større krystaller.
* Ligevægt: Til sidst når krystallen en tilstand af ligevægt, hvor hastigheden af ionvedhæftning og -løsgørelse er ens, hvilket fører til en stabil, veldefineret krystalstruktur.
Faktorer, der påvirker krystalstørrelse og -form:
* Temperatur: Højere temperaturer fører generelt til mindre krystaller.
* Kølehastighed: Langsom afkøling giver mulighed for at danne større krystaller.
* Koncentration af ioner: Højere koncentrationer fører til større krystaller.
* Tilstedeværelse af urenheder: Urenheder kan forstyrre det almindelige krystalgitter og påvirke størrelse og form.
Eksempel:
Overvej bordsalt (NaCl). Natriumioner (Na+) og chloridioner (Cl-) tiltrækker hinanden på grund af deres modsatte ladninger. De arrangerer sig selv i et regulært kubisk gitter, hvilket maksimerer tiltrækning og minimerer energi. Dette fører til dannelsen af store, kubiske krystaller af bordsalt.
Sammenfattet driver den stærke elektrostatiske tiltrækning mellem modsat ladede ioner, kombineret med deres tendens til at minimere deres energi, dannelsen af store, ordnede krystaller.
Sidste artikelHCl og jernpulverreaktion:Kemi, produkter og observationer
Næste artikelJernoxider:formler, typer og egenskaber
 Varme artikler
Varme artikler
-
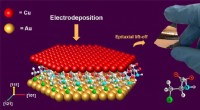 Forskere bruger aminosyrer til at dyrke højtydende kobber tynde filmKobbertynde film fremstilles ved elektroaflejring af kobber, Cu (111), på et selvsamlet organisk monolag af aminosyren L-cystein på guld, Au (111). Kredit:Bin Luo For første gang, forskere fra Mis
Forskere bruger aminosyrer til at dyrke højtydende kobber tynde filmKobbertynde film fremstilles ved elektroaflejring af kobber, Cu (111), på et selvsamlet organisk monolag af aminosyren L-cystein på guld, Au (111). Kredit:Bin Luo For første gang, forskere fra Mis -
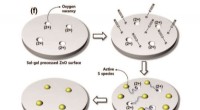 Realisering af farvefilterfri billedsensorerSkematisk mekanisme for S-doping af sol-gel-behandlet ZnO-film. Spin-coated thiocyanation (SCN?) omdannes til aktive S arter ved varmebehandling og migreres til ilt ledige steder ved elektrostatisk kr
Realisering af farvefilterfri billedsensorerSkematisk mekanisme for S-doping af sol-gel-behandlet ZnO-film. Spin-coated thiocyanation (SCN?) omdannes til aktive S arter ved varmebehandling og migreres til ilt ledige steder ved elektrostatisk kr -
 Uran afslører sin sande naturKredit:EPFL/EML De fleste mennesker kender til uran som brændstof til atomkraftværker. Og selvom det er den mest almindelige applikation, dette element bruges også på mange andre områder, såsom fa
Uran afslører sin sande naturKredit:EPFL/EML De fleste mennesker kender til uran som brændstof til atomkraftværker. Og selvom det er den mest almindelige applikation, dette element bruges også på mange andre områder, såsom fa -
 Løsningsbehandlede OLED'er baner vejen for fremtidige belysningsapplikationerKredit:Shutterstock Før det kan overtage vores gader og hjem, OLED-belysning skal gøres mere tilgængelig. SOLEDLIGHT-projektet har udviklet nye flerlags OLEDer takket være en ny proces, der lover
Løsningsbehandlede OLED'er baner vejen for fremtidige belysningsapplikationerKredit:Shutterstock Før det kan overtage vores gader og hjem, OLED-belysning skal gøres mere tilgængelig. SOLEDLIGHT-projektet har udviklet nye flerlags OLEDer takket være en ny proces, der lover
- Hvordan påvirker de gældende vindmønstre klima?
- Hvorfor er Deneb -stjernen meget lysere end Pollux Star?
- Hvilken er en grund til, at celler blev drevet?
- Hvilken binding dannes, når elektroner er gået tabt af et atom og fået et andet atom?
- Hvorfor får Gardenia Plant sorte blade?
- En opfordring til at tilføje et velfærdsindeks til nationale økonomiske mål


