Hvorfor argon er inert:Forståelse af chlors manglende reaktion
Her er hvorfor:
* Ædelgasser har en fuld ydre skal af elektroner. Dette gør dem utroligt stabile og ureaktive. De behøver ikke at vinde eller miste elektroner for at opnå en stabil konfiguration.
* Klor er på den anden side et halogen. Den har syv elektroner i sin ydre skal og ønsker at få én mere for at opnå en stabil oktet.
* For at reagere skal klor trække en elektron væk fra argon. Argons fulde ydre skal gør det dog meget vanskeligt at fjerne en elektron.
Derfor kan klor ikke overvinde stabiliteten af argons elektronkonfiguration, og der sker ingen reaktion.
Sidste artikelForbindelser vs. formler:Forstå forskellen
Næste artikelBlandinger:Forståelse af sammensætningen af stoffer
 Varme artikler
Varme artikler
-
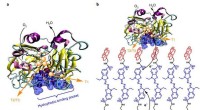 Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side
Forbedring af elektronoverførsel i enzymatiske biobrændselscellerDen som designet poly(pyrr)–ABTS–pyr film. en, Repræsentationer af Trametes versicolor Lac med den hydrofobe bindingslomme orienteret mod bunden af siden og T1 kobberstedet placeret på den ene side -
 Byg en præcis Krypton Atom-model:Trin-for-trin-vejledningAf Derek M. Kwait Opdateret 24. marts 2022 Krypton, en ædelgas med atomnummer 36, er bedst kendt som Supermans kryptonit, men dens kemi er lige så fascinerende. At forstå dens atomare struktur låser
Byg en præcis Krypton Atom-model:Trin-for-trin-vejledningAf Derek M. Kwait Opdateret 24. marts 2022 Krypton, en ædelgas med atomnummer 36, er bedst kendt som Supermans kryptonit, men dens kemi er lige så fascinerende. At forstå dens atomare struktur låser -
 Hæmatitbaserede nanotrådsstrukturer for at forbedre sol-til-brændstofkonvertering i fotoelektroke…Et materiale til brug i fotoelektrokemisk vandspaltning, der ikke kun er billigere end eksisterende alternativer, men øger både effektiviteten og outputtet af processen. Kredit:ICN2 ICN2-forskere
Hæmatitbaserede nanotrådsstrukturer for at forbedre sol-til-brændstofkonvertering i fotoelektroke…Et materiale til brug i fotoelektrokemisk vandspaltning, der ikke kun er billigere end eksisterende alternativer, men øger både effektiviteten og outputtet af processen. Kredit:ICN2 ICN2-forskere -
 Højeffektiv katalysator forbedrer den elektriske reduktionsydelse af kuldioxidKredit:CC0 Public Domain Elektrokemisk omdannelse af kuldioxid (CO 2 ) til brændstoffer og råvarer med værditilvækst, ideelt hvis drevet af vedvarende elektricitet, giver en rute til at reducere
Højeffektiv katalysator forbedrer den elektriske reduktionsydelse af kuldioxidKredit:CC0 Public Domain Elektrokemisk omdannelse af kuldioxid (CO 2 ) til brændstoffer og råvarer med værditilvækst, ideelt hvis drevet af vedvarende elektricitet, giver en rute til at reducere
- Natriumkarbonatkrystallisationsvand:Forståelse af hydrater
- Hvilke materialer beskytter magnetiske felter effektivt?
- Hvad mobiltelefoner betyder for flygtninge
- Opdagelse af en ny livsform:En forskerprotokol
- Martian Image:højdedragene i South Séítah
- Fiat Chrysler og fagforeningen indgår foreløbig kontrakt i USA


