Stærk syre-basetitrering:Produkter og reaktionsforklaring
Her er hvorfor:
* Stærk syre: Dissocierer fuldstændigt i vand og frigiver H+ ioner.
* Stærk base: Dissocierer fuldstændigt i vand og frigiver OH-ioner.
Når en stærk syre og en stærk base reagerer, reagerer H+ ionerne fra syren med OH- ionerne fra basen og danner vand (H2O). De resterende ioner, som er kationen fra basen og anionen fra syren, kombineres og danner et salt.
Eksempel:
* Saltsyre (HCl) + Natriumhydroxid (NaOH) → Natriumchlorid (NaCl) + Vand (H2O)
I dette eksempel:
* HCl er den stærke syre, der frigiver H+ og Cl-.
* NaOH er den stærke base, der frigiver Na+ og OH-.
* H+ og OH- kombineres for at danne vand.
* Na+ og Cl- kombineres for at danne natriumchlorid, et salt.
Nøglepunkter:
* Reaktionen er en neutraliseringsreaktion, da syren og basen neutraliserer hinanden.
* Det resulterende salt er normalt neutralt (ikke surt eller basisk), men nogle salte kan have let sure eller basiske egenskaber afhængigt af den anvendte syre og base.
* pH ved ækvivalenspunktet (hvor syren og basen har neutraliseret hinanden fuldstændigt) er tæt på 7 for stærke syrestærke basetitreringer.
 Varme artikler
Varme artikler
-
 Billig tin pakker et stort slag for fremtiden for superkapacitorerForskere dopede koboltoxid med tin for at skabe en mere effektiv elektrode til brug i superkapacitorer. Dette mikroskopiske billede viser det nye materiale på grafenfilm. Kredit:JIa Zhu/Penn State
Billig tin pakker et stort slag for fremtiden for superkapacitorerForskere dopede koboltoxid med tin for at skabe en mere effektiv elektrode til brug i superkapacitorer. Dette mikroskopiske billede viser det nye materiale på grafenfilm. Kredit:JIa Zhu/Penn State -
 Sådan sammenlignes syrestyrke af forbindelser:En praktisk vejledningAf Marissa Robert | Opdateret 30. august 2022 At bestemme, om en forbindelse er sur, basisk eller neutral, kan være så simpel som en lakmustest. Rangering af surhedsgraden af to eller flere forbind
Sådan sammenlignes syrestyrke af forbindelser:En praktisk vejledningAf Marissa Robert | Opdateret 30. august 2022 At bestemme, om en forbindelse er sur, basisk eller neutral, kan være så simpel som en lakmustest. Rangering af surhedsgraden af to eller flere forbind -
 Tarmbakterier er nøglen til fremstilling af universalblodKredit:Wikimedia Commons I januar, rasende storme forårsagede medicinske nødsituationer langs den amerikanske østkyst, får Røde Kors til at udsende en hasteopfordring til bloddonationer. Nationens
Tarmbakterier er nøglen til fremstilling af universalblodKredit:Wikimedia Commons I januar, rasende storme forårsagede medicinske nødsituationer langs den amerikanske østkyst, får Røde Kors til at udsende en hasteopfordring til bloddonationer. Nationens -
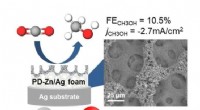 Omdannelse af kuldioxid til methanol(Venstre) Skematisk fremstilling af methanol ved elektrokatalytisk reduktion af kuldioxid ved brug af PD-Zn/Ag skumkatalysatoren. (Højre) Scanning elektronmikroskopi billede af overfladen af PD-Zn/A
Omdannelse af kuldioxid til methanol(Venstre) Skematisk fremstilling af methanol ved elektrokatalytisk reduktion af kuldioxid ved brug af PD-Zn/Ag skumkatalysatoren. (Højre) Scanning elektronmikroskopi billede af overfladen af PD-Zn/A


