Beregning af masse i kemiske reaktioner:Natriumoxid og vand
Det er vigtigt at bemærke: Du kan ikke direkte tilføje masserne af natriumoxid og vand for at få massen af produktet af deres reaktion. Her er hvorfor:
* Kemisk reaktion: Natriumoxid og vand reagerer for at danne natriumhydroxid (NaOH):
Na20 + H2O → 2 NaOH
* Bevarelse af messen: I en kemisk reaktion er den samlede masse af reaktanterne (udgangsmaterialerne) lig med den samlede masse af produkterne (dannte stoffer).
For at beregne massen af produkterne skal du bruge:
1. Mængderne af natriumoxid og vand: Du skal vide, hvor meget af hver reaktant du starter med.
2. Stykiometri: Du skal bruge den afbalancerede kemiske ligning til at finde ud af, hvor meget natriumhydroxid der produceres fra de givne mængder natriumoxid og vand.
Eksempel:
Lad os sige, at du har 10 gram natriumoxid og 5 gram vand. Sådan griber du problemet an:
1. Konverter gram til mol:
* Mol Na2O =(10 g Na2O) / (61,98 g/mol Na2O) =0,161 mol Na2O
* Mol H2O =(5 g H2O) / (18,02 g/mol H2O) =0,277 mol H2O
2. Bestem begrænsende reaktant:
* Den begrænsende reaktant er den, der bliver brugt først, hvilket begrænser mængden af dannet produkt.
* Fra den afbalancerede ligning reagerer 1 mol Na₂O med 1 mol H₂O.
* Da vi har færre mol Na₂O, er det den begrænsende reaktant.
3. Beregn mol produkt:
* Mol NaOH =(0,161 mol Na2O) * (2 mol NaOH / 1 mol Na2O) =0,322 mol NaOH
4. Konverter mol produkt til gram:
* Masse af NaOH =(0,322 mol NaOH) * (40,00 g/mol NaOH) =12,88 gram NaOH
Derfor ville massen af produktet (natriumhydroxid) være 12,88 gram.
Vigtig bemærkning: Dette er blot et eksempel. Du bliver nødt til at tilpasse beregningerne baseret på de specifikke mængder natriumoxid og vand, du arbejder med.
 Varme artikler
Varme artikler
-
 Hæmmer eller fremmer zink vækst af nyresten? Godt, beggeKredit:CC0 Public Domain Der skete en sjov ting på vejen til at opdage, hvordan zink påvirker nyresten - to forskellige teorier dukkede op, hver modsiger hinanden. Et:Zink stopper væksten af de
Hæmmer eller fremmer zink vækst af nyresten? Godt, beggeKredit:CC0 Public Domain Der skete en sjov ting på vejen til at opdage, hvordan zink påvirker nyresten - to forskellige teorier dukkede op, hver modsiger hinanden. Et:Zink stopper væksten af de -
 Akustisk fokusering til at samle mikroplast i vandKredit:CC0 Public Domain Mikroplast har fået meget opmærksomhed på det seneste på grund af deres vanskeligheder med at fjerne dem fra miljøet. Sigter og filtrering er i øjeblikket den fremherskend
Akustisk fokusering til at samle mikroplast i vandKredit:CC0 Public Domain Mikroplast har fået meget opmærksomhed på det seneste på grund af deres vanskeligheder med at fjerne dem fra miljøet. Sigter og filtrering er i øjeblikket den fremherskend -
 Ny metode retter sig mod sygdomsfremkaldende proteiner til destruktionWeiping Tang, professor i farmaci og kemi ved University of Wisconsin-Madison. Kredit:Sally Griffith-Oh Forskere ved University of Wisconsin-Madison har udviklet en måde at bruge en celles eget ge
Ny metode retter sig mod sygdomsfremkaldende proteiner til destruktionWeiping Tang, professor i farmaci og kemi ved University of Wisconsin-Madison. Kredit:Sally Griffith-Oh Forskere ved University of Wisconsin-Madison har udviklet en måde at bruge en celles eget ge -
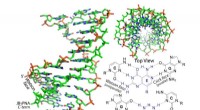 Syntetisk molekyle invaderer dobbeltstrenget DNAUdviklet af forskere ved Carnegie Mellon University, denne janus gamma peptid nukleinsyre (PNA) kan invadere den dobbelte helix af DNA og RNA. Kredit:Carnegie Mellon University Carnegie Mellon Uni
Syntetisk molekyle invaderer dobbeltstrenget DNAUdviklet af forskere ved Carnegie Mellon University, denne janus gamma peptid nukleinsyre (PNA) kan invadere den dobbelte helix af DNA og RNA. Kredit:Carnegie Mellon University Carnegie Mellon Uni
- Hvad er Glucose fremstillet af?
- Hvorfor skal folk bruge solenergi?
- MicroMESH:Et mikroskopisk polymert netværk til at angribe glioblastoma multiforme
- Hvilken farvestjerne er Epsilon Sagittarii?
- Grønvasker kvarterer med lav trafik? Her er hvad beviserne siger
- Hvad er egenskaber, der beskriver udseendet af stof?


