Syntetisk molekyle invaderer dobbeltstrenget DNA
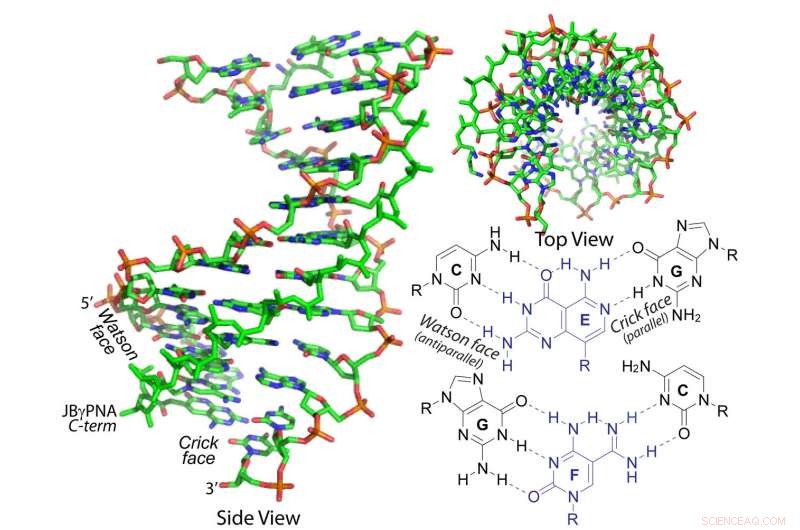
Udviklet af forskere ved Carnegie Mellon University, denne janus gamma peptid nukleinsyre (PNA) kan invadere den dobbelte helix af DNA og RNA. Kredit:Carnegie Mellon University
Carnegie Mellon University forskere har udviklet et syntetisk molekyle, der kan genkende og binde sig til dobbeltstrenget DNA eller RNA under normale fysiologiske forhold. Molekylet kan udgøre en ny platform for udvikling af metoder til diagnosticering og behandling af genetiske tilstande. Deres resultater er offentliggjort i Kommunikationskemi .
Arbejdet blev udført af et internationalt team af eksperter, herunder Carnegie Mellon professor i kemi Danith Ly, en ekspert i peptidnukleinsyredesign, kemi postdoc Shivaji Thadke og kemi kandidatstuderende Dinithi Perera, Kemiprofessor og ekspert i kernemagnetisk resonans Roberto Gil, og Arnab Mukherjee, en datalog ved The Indian Institute of Science Education and Research i Pune.
"Da den dobbeltspiralformede struktur af DNA først blev belyst af Watson og Crick, videnskabsmænd har forsøgt at designe molekyler, der kan binde sig til DNA og tillade en at kontrollere strømmen af genetisk information, " sagde Ly. "Dette er det første bifaciale molekyle, der kan invadere dobbeltstrenget DNA eller RNA under biologisk relevante forhold."
DNA, som indeholder al en organismes genetiske information, består af to strenge af nukleotider. Nukleotiderne forbindes med hinanden ved hjælp af hydrogenbindinger, danner en spiralformet kæde af Watson-Crick basepar. Mens disse basepar giver en relativt simpel kode til vores genetiske information, Det er svært at komme ind i dobbelthelixen for at ændre koden på grund af de stærke bindinger mellem baseparrene.
Ly og hans kolleger ved Carnegie Mellon University's Institute for Biomolecular Design and Discovery (IBD) og Center for Nucleic Acids Science and Technology (CNAST) er førende inden for design og udvikling af gamma-peptidnukleinsyrer (gamma-PNA'er). Syntetiske analoger til DNA og RNA, gamma-PNA'er kan programmeres til at binde til det genetiske materiale (DNA eller RNA), der forårsager sygdom, giver dem mulighed for at søge efter skadelige sekvenser og binde sig til dem for at forhindre et gen i at fungere dårligt.
Gruppen har skabt dobbeltsidede gamma-PNA'er kaldet Janus gamma-PNA'er. Opkaldt efter den to-ansigtede romerske gud, Janus PNA'er er i stand til at genkende og binde til begge strenge af et DNA- eller RNA-molekyle.
Begrebet bifacial genkendelse, som er grundlaget for Janus gamma PNA'er, blev først udtænkt for mere end to årtier siden af Jean-Marie Lehn, en nobelprismodtager kendt for sit arbejde inden for supramolekylær kemi, og forklaret af andre forskere på området.
Fremme af denne forskning er blevet holdt tilbage af to forhindringer. Først, forskere havde kun været i stand til at lave et lille antal Janus-baser, og disse baser varierede betydeligt i form og størrelse. Disse begrænsninger betød, at de forskellige Janus-baser kun kunne genkende gentagelser af det samme sæt af basepar og ikke kunne bruges sammen som byggesten til at genkende mere komplekse sekvenser i DNA eller RNA.
For det andet det var svært at syntetisere Janus-baser til kanoniske basepar. Den komplementære karakter af de to sider af Janus-baserne fik molekylerne til at hybridisere og binde sig til hinanden, forhindrer dem i at blive inkorporeret i DNA og RNA.
I den aktuelle undersøgelse, Ly og kolleger overvinder disse forhindringer. De skabte et helt nyt sæt af bifacial nukleinsyregenkendelseselementer, 16 i alt, der stod for enhver mulig kombination af nukleobaser, der kunne findes i den genetiske kode. Janus gamma PNA'erne kan bruges til at genkende enhver kombination af basepar og blandes og matches for at detektere og binde til komplekse genetiske sekvenser.
Thadke løste det kemiske synteseproblem ved at udtænke en ny opløsnings- og fastfase-syntesemetode til at udvikle Janus gamma PNA'er. Han implementerede også et trick, der ligger i den spiralformede præorganisering i rygraden af gamma-PNA for at forhindre selvkomplementære Janus-baser i at hybridisere til hinanden.
Disse nye Janus gamma PNA'er har en ekstraordinær høj bindingsenergi og er de første til at være i stand til at invadere en kanonisk baseparret DNA eller RNA dobbelthelix ved en fysiologisk relevant ionstyrke og temperatur.
Det gør de ved at drage fordel af, når dobbeltstrengede DNA- og RNA-molekyler "ånder", og bindingerne mellem baseparrene åbner sig i brøkdele af et sekund. Når dette sker, Janus PNA indsætter sig selv mellem de adskilte strenge. Hvis baseparrene ikke stemmer overens, Janus PNA udstødes fra DNA-molekylet. Men hvis de matcher, Janus PNA binder til begge strenge af molekylet.
Janus gamma PNA'er har en bred vifte af biologiske og biomedicinske anvendelser. De kan designes til at målrette genomisk DNA til genredigering og transkriptionel regulering. De kunne også designes til at binde sekvensspecifikt og selektivt til de sekundære og tertiære strukturer af RNA, noget, som traditionelle antisense-midler og ligander med små molekyler ikke er i stand til. For eksempel, Janus gamma PNA'erne kunne programmeres til at binde til RNA-gentagne udvidelser, som kan føre til nye behandlinger for en række neuromuskulære og neurodegenerative lidelser, herunder myotonisk dystrofi type 1 og Huntingtons sygdom, eller til ikke-kodende RNA'er, herunder patogens ribosomale og telomerase-RNA, at bekæmpe genetiske og infektionssygdomme.
Teknologien udforskes af startups såvel som af farmaceutiske virksomheder med henblik på terapeutisk udvikling.
 Varme artikler
Varme artikler
-
 Ny teknik bringer studiet af molekylær konfiguration ind i det mikroskopiske domæneRohit Bhargava med postdoktor Kevin Yeh, der designede det brugerdefinerede infrarøde mikroskop, der blev brugt til denne undersøgelse. Dette foto er taget i februar 2020. Kredit:L. Brian Stauffer, Un
Ny teknik bringer studiet af molekylær konfiguration ind i det mikroskopiske domæneRohit Bhargava med postdoktor Kevin Yeh, der designede det brugerdefinerede infrarøde mikroskop, der blev brugt til denne undersøgelse. Dette foto er taget i februar 2020. Kredit:L. Brian Stauffer, Un -
 Field Trip-ideer til High School ChemistryFeltrejser er en fremragende måde at understrege lektioner og hjælpe eleverne med at forstå, at det, de lærer i klasseværelset, kan anvendes til det virkelige liv. Når man udvikler feltrejser for kemi
Field Trip-ideer til High School ChemistryFeltrejser er en fremragende måde at understrege lektioner og hjælpe eleverne med at forstå, at det, de lærer i klasseværelset, kan anvendes til det virkelige liv. Når man udvikler feltrejser for kemi -
 Mikrobielt tyveri muliggør nedbrydning af metan, giftig methylkviksølvForskere fik ny indsigt i de mekanismer, som nogle methan-fødende bakterier kaldet metanotrofer bruger til at nedbryde toksinet methylkviksølv. Kredit:Andy Sproles/ORNL, US Department of Energy; Jerem
Mikrobielt tyveri muliggør nedbrydning af metan, giftig methylkviksølvForskere fik ny indsigt i de mekanismer, som nogle methan-fødende bakterier kaldet metanotrofer bruger til at nedbryde toksinet methylkviksølv. Kredit:Andy Sproles/ORNL, US Department of Energy; Jerem -
 Sådan beregnes MmolFor blot deres beregninger at oprette kemikere en standardenhed for antallet af atomer i en bestemt forbindelse involveret i en reaktion eller en anden kemisk proces. De definerer en mol (mol) som
Sådan beregnes MmolFor blot deres beregninger at oprette kemikere en standardenhed for antallet af atomer i en bestemt forbindelse involveret i en reaktion eller en anden kemisk proces. De definerer en mol (mol) som
- Sådan fungerer Pi
- Supersonisk spray giver nyt nanomateriale til bøjeligt, bærbar elektronik
- Vil terrorisme fortsætte med at falde i 2019?
- Forskere ser blodkar udvikle sig i hele zebrafiskembryoner
- Hvor meget vil vores emissioner have indflydelse på det fremtidige istab i Antarktis?
- Hvorfor Chuck Yeager var den største pilot nogensinde


