Forståelse af grundlæggende forbindelser og hydroxidiondannelse
Grundlæggende forbindelser:
* Arrhenius-baser: Disse er den klassiske definition af baser. De producerer OH-ioner direkte, når de opløses i vand. Eksempler omfatter NaOH (natriumhydroxid) og KOH (kaliumhydroxid).
* Brønsted-Lowry Baser: Disse er mere generelle. De accepterer protoner (H+) fra vandmolekyler, som danner OH-ioner. Dette inkluderer mange forbindelser, der ikke har OH-grupper i deres struktur. Eksempler omfatter NH3 (ammoniak) og Na2CO3 (natriumcarbonat).
* Lewis-baser: Disse er den bredeste definition af baser. De donerer elektronpar, hvilket kan føre til OH-dannelse indirekte i nogle tilfælde.
Vigtige pointer:
* Ikke alle basisforbindelser producerer OH- direkte: Mange basisforbindelser, især Brønsted-Lowry baser, har ikke direkte OH-ioner i deres struktur. De skaber OH- gennem reaktioner med vand.
* Forbindelsens natur har betydning: Hvorvidt en basisk forbindelse producerer OH- afhænger af dens specifikke kemiske egenskaber og hvordan den interagerer med vand.
Eksempel:
* Ammoniak (NH3) er en base: Det reagerer med vand og danner ammoniumioner (NH4+) og hydroxidioner (OH-):
NH3 + H2O ⇌ NH4+ + OH-
Konklusion:
Mens nogle basiske forbindelser direkte producerer OH-ioner, gør mange andre det indirekte gennem reaktioner med vand. At forstå de forskellige definitioner af baser og deres interaktioner med vand er afgørende for at forstå, hvordan OH-ioner dannes.
 Varme artikler
Varme artikler
-
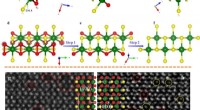 Kontrollerbar overfladedefektteknik på overgangsmetaltrichalcogenidFigur (a-f) viser den skematiske proces for omdannelsen af monoklint zirconiumtrisulfid, ZrS3 (ICCD PDF nr. 30-1498) til sekskantet zirconiumsulfid, ZrS2 (ICCD PDF-nr. 11-0679) fra [010] (a-c) og [0
Kontrollerbar overfladedefektteknik på overgangsmetaltrichalcogenidFigur (a-f) viser den skematiske proces for omdannelsen af monoklint zirconiumtrisulfid, ZrS3 (ICCD PDF nr. 30-1498) til sekskantet zirconiumsulfid, ZrS2 (ICCD PDF-nr. 11-0679) fra [010] (a-c) og [0 -
 Beregn den indledende reaktionshastighed:En trin-for-trin guideGarsya/iStock/GettyImages Kinetik er den gren af fysisk kemi, der studerer hastigheden af kemiske reaktioner. I modsætning hertil fortæller termodynamikken os, hvilken retning af reaktionen der foret
Beregn den indledende reaktionshastighed:En trin-for-trin guideGarsya/iStock/GettyImages Kinetik er den gren af fysisk kemi, der studerer hastigheden af kemiske reaktioner. I modsætning hertil fortæller termodynamikken os, hvilken retning af reaktionen der foret -
 Forskere opretter vandfiltreringsmembraner, der kan rense sig selvEn kunstners gengivelse af lysinduceret selvrensning af en forurenet membran. Kredit:Argonne National Laboratory Forskere ved Department of Energys (DOE) Argonne National Laboratory har udviklet e
Forskere opretter vandfiltreringsmembraner, der kan rense sig selvEn kunstners gengivelse af lysinduceret selvrensning af en forurenet membran. Kredit:Argonne National Laboratory Forskere ved Department of Energys (DOE) Argonne National Laboratory har udviklet e -
 Befri oceanerne for plastik ved at omdanne affaldet til værdifuldt brændstofJames Holm (billedet) og Swaminathan Ramesh, Ph.D., gik sammen om at udvikle en mobil reaktor (også på billedet) til at omdanne affaldsplastik til brændstof. Kredit:Claudia Rocha Milliarder af pou
Befri oceanerne for plastik ved at omdanne affaldet til værdifuldt brændstofJames Holm (billedet) og Swaminathan Ramesh, Ph.D., gik sammen om at udvikle en mobil reaktor (også på billedet) til at omdanne affaldsplastik til brændstof. Kredit:Claudia Rocha Milliarder af pou
- Hvilke dyr lever i et egetræ?
- Hvorfor er folk besat af Space Moons -stjerner universet osv.?
- Når brændende benzin i motorkøretøjer 2 gasser dannes, som bidrager til surt regn, hvad er gasse…
- Hvad er pollenlevbarhed?
- Hvad opdagede Voyager?
- Hvad kan du sige om energien fra en bold ved Point -frigivelse sammenlignet med toppen af dens afv…


