Ammoniakopløselighed i vand:Hydrogenbinding og polaritet forklaret
1. Hydrogenbinding:
* Ammoniak har et ensomt elektronpar på nitrogenatomet, hvilket gør det i stand til at danne brintbindinger med vandmolekyler.
* Disse hydrogenbindinger er stærke intermolekylære kræfter, der bidrager væsentligt til ammoniakens opløselighed i vand.
2. Polaritet:
* Ammoniakmolekylet er polært på grund af elektronegativitetsforskellen mellem nitrogen- og brintatomer.
* Vand er også et polært molekyle.
* Tiltrækningen mellem den positive ende af vandmolekylet (brint) og den negative ende af ammoniakmolekylet (nitrogen) øger opløseligheden.
3. Evne til at danne ammoniumioner:
* Når ammoniak opløses i vand, reagerer det med vandmolekyler og danner ammoniumioner (NH₄⁺) og hydroxidioner (OH⁻):
NH3(g) + H2O(l) ⇌ NH4+(vandig) + OH⁻(vandig)
* Denne reaktion er en ligevægtsreaktion, og dannelsen af ammoniumioner øger yderligere opløseligheden af ammoniak i vand.
4. Lille størrelse:
* Ammoniakmolekyler er relativt små, hvilket giver dem mulighed for nemt at interagere med vandmolekyler og opløses.
Samlet set:
Kombinationen af hydrogenbinding, polaritet, evnen til at danne ammoniumioner og lille størrelse gør ammoniak meget opløseligt i vand.
Bemærk: Mens ammoniak er meget opløseligt i vand, er det stadig en gas ved stuetemperatur. De opløste ammoniakmolekyler danner dog let ammoniumioner, som er positivt ladede og derfor forbliver i opløsning.
 Varme artikler
Varme artikler
-
 Medicinske kemiske gennembrud kan føre til bedre lægemidlerKemiprofessor W. Dean Harman ledede et team, der udviklede en ny metode til fremstilling af lægemidler. Kredit:Dan Addison, Universitetets kommunikation Medicin er udviklet til at fungere godt for
Medicinske kemiske gennembrud kan føre til bedre lægemidlerKemiprofessor W. Dean Harman ledede et team, der udviklede en ny metode til fremstilling af lægemidler. Kredit:Dan Addison, Universitetets kommunikation Medicin er udviklet til at fungere godt for -
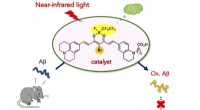 Nær-infrarøde fotoaktiverbare oxygeneringskatalysatorer af amyloidpeptidKredit:Japan Science and Technology Agency (JST) En ny, Der er udviklet biokompatibel fotooxygeneringskatalysator, der selektivt kan ilte og nedbryde den patogene aggregering af Alzheimers sygdom
Nær-infrarøde fotoaktiverbare oxygeneringskatalysatorer af amyloidpeptidKredit:Japan Science and Technology Agency (JST) En ny, Der er udviklet biokompatibel fotooxygeneringskatalysator, der selektivt kan ilte og nedbryde den patogene aggregering af Alzheimers sygdom -
 Video:Blev din katalysator stjålet? Her er hvorforKredit:The American Chemical Society Katalysatorer reducerer giftige bilemissioner, og, ifølge U.S. Environmental Protection Agency, de er en af de største miljøopfindelser nogensinde. I dag, t
Video:Blev din katalysator stjålet? Her er hvorforKredit:The American Chemical Society Katalysatorer reducerer giftige bilemissioner, og, ifølge U.S. Environmental Protection Agency, de er en af de største miljøopfindelser nogensinde. I dag, t -
 Accelereret analyse af stabiliteten af komplekse legeringerProfessor dr. Alfred Ludwig, Dr. Yujiao Li, Alan Savan og dr. Aleksander Kostka (fra forside til bagside). Kredit:RUB, Marquard Materialeforskere ved Ruhr-Universität Bochum er i stand til at afgø
Accelereret analyse af stabiliteten af komplekse legeringerProfessor dr. Alfred Ludwig, Dr. Yujiao Li, Alan Savan og dr. Aleksander Kostka (fra forside til bagside). Kredit:RUB, Marquard Materialeforskere ved Ruhr-Universität Bochum er i stand til at afgø
- Ny teknik inkorporerer kulstof-14 i et enkelt trin for sikrere og mere effektiv opdagelse af lægemi…
- Hvor mange milliamperer i 1 K?
- Simuleret mikrotyngdekraft påvirker søvn og fysiologiske rytmer, viser undersøgelse
- Hjemmelavet Heat Tape
- Hvilken enhed består af to separate spiraler, der er pakket rundt om en jernring?
- Pinterest rapporterer mindre tab i 1. kvartal, men resultaterne trækker lager


