Beregn den indledende reaktionshastighed:En trin-for-trin guide
Garsya/iStock/GettyImages
Kinetik er den gren af fysisk kemi, der studerer hastigheden af kemiske reaktioner. I modsætning hertil fortæller termodynamikken os, hvilken retning af reaktionen der foretrækkes, uden at afsløre dens reaktionshastighed. Nogle reaktioner kan være termodynamisk begunstigede, men kinetisk ugunstige.
For eksempel ved omdannelsen af diamant til grafit har grafit en lavere fri energi end diamant, så omdannelsen er termodynamisk begunstiget. Der er dog en stor aktiveringsbarriere for diamant til at bryde og omforme alle bindinger til den mere stabile grafitkonfiguration, så denne reaktion er kinetisk ugunstig og vil faktisk ikke forekomme.
Reaktionshastighed
Reaktionshastighed
reaktionshastigheden er et mål for, hvor hurtigt produkterne dannes og reaktanterne forbruges, så du kan bestemme det ved at måle ændringen i koncentrationen af produkter eller reaktanter, over en periode. Overvej en generel kemisk reaktion:
aA + bB ———————–> cC + dD
Reaktionshastigheden kan skrives som:
Ændret fra https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_Physical_and_Theoretical_Chemistry/Kinetics/Reaction_Rates/Experimental_Determination_of_Kinetcs_PReaction_Rates
For eksempel reaktionshastigheden for:
2 NO(g) + 2 H2 (g) ———————> N2(g) + 2 H2O(g)
er givet af
Tilpasset fra https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_Physical_and_Theoretical_Chemistry/Kinetics/Reaction_Rates/Experimental_Determination_of_Kinetcs_Preaction_Rates For at bestemme hastigheden af denne reaktion ved eksperiment kan du måle koncentrationen af H2 på forskellige tidspunkter af reaktionen og plotte den mod tiden som følger:
Ændret fra https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_Physical_and_Theoretical_Chemistry/Kinetics/Reaction_Rates/Experimental_Determination_of_Kinetcs_PReaction_Rates
Ændret fra https://chem.libretexts.org/Bookshelves/Physical_and_Theoretical_Chemistry_Textbook_Maps/Supplemental_Modules_Physical_and_Theoretical_Chemistry/Kinetics/Reaction_Rates/Experimental_Determination_of_Kinetcs_PReaction_Rates
Den gennemsnitlige reaktionshastighed er en tilnærmelse af reaktionshastigheden i et tidsinterval og kan betegnes med:
Ændret fra https://www.chem.purdue.edu/gchelp/howtosolveit/Kinetics/CalculatingRates.html#InitialRate
Den øjeblikkelige reaktionshastighed er defineret som reaktionshastigheden på et eller andet tidspunkt. Det er en differentialsats og kan udtrykkes ved:
Ændret fra https://www.chem.purdue.edu/gchelp/howtosolveit/Kinetics/CalculatingRates.html#InitialRate
Hvor d[H2]/dt er hældningen for kurven for koncentration af H2 versus tiden på tidspunktet t.
Den indledende reaktionshastighed er den øjeblikkelige hastighed ved starten af reaktionen, når t =0. I dette tilfælde er enheden for gennemsnitlig, øjeblikkelig og initial reaktionshastighed er M/s.
Satslov
Satslov
I de fleste tilfælde er reaktionshastigheden afhængig af koncentrationen af de forskellige reaktanter på tidspunktet t. For eksempel, i en højere koncentration af alle reaktanter, kolliderer reaktanter hyppigere og resulterer i en hurtigere reaktion. Forholdet mellem reaktionshastigheden ν(t) og koncentrationerne er defineret som hastighedsloven . Og hastighedsloven for den generelle kemiske reaktion aA + bB —————> cC + dD er:
Ændret fra https:
Hvor k er hastighedskonstanten, og potensen x og y er ordenen af reaktionen med hensyn til reaktant A og B. Hastighedsloven skal bestemmes eksperimentelt og kan ikke udledes kun ud fra støkiometrien af en afbalanceret kemisk reaktion.
Metode for indledende takster
Metode for indledende takster
Takstloven kan bestemmes ved metoden med starttakster . I denne metode udføres eksperimentet flere gange, kun ændre koncentrationen af en reaktant for hver kørsel, mens andre variabler holdes konstante. Reaktionshastigheden måles for hver kørsel for at bestemme rækkefølgen af hver reaktant i hastighedsloven.
Overvej f.eks. følgende starthastighedsdata for reaktionen:
2 NO(g) + 2 H2 (g) ———————> N2(g) + 2 H2O(g)
Tilpasset fra https://www.chemteam.info/Kinetics/WS-Kinetics-method-of-initial-rates.html
For forsøg 1 og 3 holdes koncentrationen af NO konstant, mens koncentrationen af H2 fordobles. Som følge heraf blev den indledende reaktionshastighed også fordoblet (tænk på det som 21), så du kan konkludere y =1. For forsøg 1 og 2 fordobles koncentrationen af NO, mens koncentrationen af H2 forbliver konstant. Resultatet af denne ændring er, at den oprindelige sats blev firedoblet (tænk på det som 22). Du kan derfor konkludere x =2.
Hastighedsloven for denne reaktion er derfor:
Tilpasset fra https://www.chemteam.info/Kinetics/WS-Kinetics-method-of-initial-rates.html
Og reaktionen er første orden i H2 og anden orden i NEJ.
 Varme artikler
Varme artikler
-
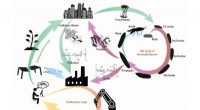 Team udvikler manglende led til cirkulær økonomi, mens de tackler globalt affaldSkematisk over det udviklede lukkede produktionskredsløb baseret på bioinspirerede kitinholdige materialer og biokonvertering i et bymiljø. Kredit:SUTD Forskere fra Singapore University of Technol
Team udvikler manglende led til cirkulær økonomi, mens de tackler globalt affaldSkematisk over det udviklede lukkede produktionskredsløb baseret på bioinspirerede kitinholdige materialer og biokonvertering i et bymiljø. Kredit:SUTD Forskere fra Singapore University of Technol -
 Håndholdt spektralanalysator gør smartphonen til et diagnostisk værktøjDen spektrale transmissions-reflektans-intensitet (TRI) -analysator fastgøres til en smartphone og analyserer patientblod, urin, eller spytprøver lige så pålideligt som klinikbaserede instrumenter, de
Håndholdt spektralanalysator gør smartphonen til et diagnostisk værktøjDen spektrale transmissions-reflektans-intensitet (TRI) -analysator fastgøres til en smartphone og analyserer patientblod, urin, eller spytprøver lige så pålideligt som klinikbaserede instrumenter, de -
 Ny forskning kan hjælpe renere energiteknologierGuangwen Zhou er professor i maskinteknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Ny forskning ledet af fakultetet ved B
Ny forskning kan hjælpe renere energiteknologierGuangwen Zhou er professor i maskinteknik ved Binghamton University, State University of New York. Kredit:Binghamton University, State University of New York Ny forskning ledet af fakultetet ved B -
 Forskere opdager vejen til at forbedre spilskiftende batterielektrodeElbilproducenter er intenst interesserede i lithium-rige batterikatoder, der kan øge rækkevidden betydeligt. En ny undersøgelse åbner en vej til at få dem til at leve op til deres løfte. Kredit:Stanfo
Forskere opdager vejen til at forbedre spilskiftende batterielektrodeElbilproducenter er intenst interesserede i lithium-rige batterikatoder, der kan øge rækkevidden betydeligt. En ny undersøgelse åbner en vej til at få dem til at leve op til deres løfte. Kredit:Stanfo
- Hvilken type bølge ville blive oprettet ved episentret?
- Ikke-hvide forskere er underrepræsenteret i videnskabelige artikler i kommunikation
- Hvad er molariteten af en opløsning, hvor 58 g NaCl opløses 1,0 L opløsning?
- Skræddersyet beskeder øger forståelsen af klimaændringer hos republikanerne
- Kigger ind i hjertet af en supernova:Simulering viser, hvordan man kan detektere en stjernekerne, de…
- Hvor mange gram nitrogendioxid skal reagere med vand for at producere 5,00x10 22 molekyler monoxid?


