Elektronplacering i kovalente bindinger:En detaljeret forklaring
Her er en mere detaljeret forklaring:
* Kovalente bindinger dannes, når to atomer deler elektroner. Disse delte elektroner tiltrækkes af kernerne i begge atomer og holder dem sammen.
* De delte elektroner er ikke fikseret på ét sted, men findes snarere i et område af rummet kaldet en "molekylær orbital." Denne orbital omgiver begge atomkerner.
* Elektrondensiteten er højest i området mellem de to kerner. Det betyder, at elektronerne er mere tilbøjelige til at blive fundet i det område.
* Formen af den molekylære orbital afhænger af de specifikke involverede atomer og de typer orbitaler, de bruger til at dele elektroner.
Tænk på det som to personer, der holder hinanden i hånden. De delte elektroner er som hænder, der er knyttet sammen, og forbinder de to personer (atomer). De er ikke permanent knyttet til nogen af personerne, men eksisterer snarere i rummet mellem dem og holder dem sammen.
 Varme artikler
Varme artikler
-
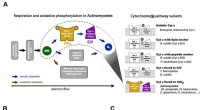 Klar til nærbilledet - en bakteries elektrontransportvejRespiration i Actinomycetes og overordnet arkitektur af Mycobacterial respiratorisk maskine CIII2CIV2SOD2. A) Den respiratoriske elektronoverførselskæde i Actinomycetes (venstre) og de 5 større prokar
Klar til nærbilledet - en bakteries elektrontransportvejRespiration i Actinomycetes og overordnet arkitektur af Mycobacterial respiratorisk maskine CIII2CIV2SOD2. A) Den respiratoriske elektronoverførselskæde i Actinomycetes (venstre) og de 5 større prokar -
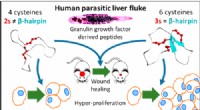 Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l
Et molekyle produceret af en thailandsk leverparasit kan være løsningen på de ikke-helende sårKredit:ACS Hver dag amputeres 12 australske diabetikere på grund af et sår, der ikke heler. Globalt set det er en hvert 30. sekund. Et molekyle produceret af en thailandsk leverparasit kan være l -
 Forskere får kontrol over syntesen af bløde molekylerKemisk og biomolekylær ingeniørprofessor Damien Guironnet, ret, og kandidatstuderende Dylan Walsh udviklede en ny teknik, der giver dem mulighed for at programmere størrelsen, form og sammensætning af
Forskere får kontrol over syntesen af bløde molekylerKemisk og biomolekylær ingeniørprofessor Damien Guironnet, ret, og kandidatstuderende Dylan Walsh udviklede en ny teknik, der giver dem mulighed for at programmere størrelsen, form og sammensætning af -
 Regn, regn, gå væk:Ny vandtætningsløsning opdagetKredit:CC0 Public Domain En ny belægningsløsning opdaget af forskere ved Simon Fraser University kan forvandle almindelige materialer til vandtætte overflader. Produktet vil være billigere at prod
Regn, regn, gå væk:Ny vandtætningsløsning opdagetKredit:CC0 Public Domain En ny belægningsløsning opdaget af forskere ved Simon Fraser University kan forvandle almindelige materialer til vandtætte overflader. Produktet vil være billigere at prod
- Hvornår forekommer respiration i planter?
- Sammenligning af flaskehalseffekt og grundlæggereffekt
- Hvad er nogle plantetilpasninger i junglen?
- Når højden af en faldet kugle mindsker, hvad sker der med dens potentielle energi?
- Hvad er urinens pH i en dehydreret person?
- Når lys passerer i en vinkel til det normale fra et materiale, hvor det er højere, hvad sker der?


