Enkeltforskydningsreaktioner:Forståelse af redoxprocesser
* Redox-reaktioner: Disse reaktioner involverer overførsel af elektroner mellem reaktanter. Den ene reaktant mister elektroner (oxidation), mens den anden får elektroner (reduktion).
* Enkeltforskydningsreaktioner: I disse reaktioner fortrænger et mere reaktivt element et mindre reaktivt element fra en forbindelse. Denne forskydning opstår, fordi det mere reaktive element har en stærkere tendens til at tabe elektroner (oxidation), og det mindre reaktive element har en stærkere tendens til at få elektroner (reduktion).
Eksempel:
Overvej reaktionen mellem zink og kobber(II)sulfat:
Zn(s) + CuSO4(aq) → ZnSO4(aq) + Cu(s)
* Zink (Zn) er mere reaktiv end kobber (Cu) .
* Zink taber elektroner og bliver oxideret og danner Zn²⁺ ioner.
* Kobber(II)-ioner (Cu²⁺) vinder elektroner og bliver reduceret og danner kobbermetal (Cu) .
Nøgleafhentning: Fordi enkelte forskydningsreaktioner involverer en ændring i oxidationstilstande af de involverede elementer, er de altid redoxreaktioner.
 Varme artikler
Varme artikler
-
 Ny syntetisk metode til vandstabile perovskitterVandstabil perovskitprøve under syntetisk tilstand, som udviser cyangrøn farve i basismedier under syntese under UV-lys. Kredit:UNIST Forskere i Sydkorea har præsenteret en nem og omkostningseffek
Ny syntetisk metode til vandstabile perovskitterVandstabil perovskitprøve under syntetisk tilstand, som udviser cyangrøn farve i basismedier under syntese under UV-lys. Kredit:UNIST Forskere i Sydkorea har præsenteret en nem og omkostningseffek -
 Video:Hvad er flammejetting?Kredit:The American Chemical Society Vi ved, at brændstoffer som benzin og alkohol kan brænde. Men nogle gange, når forholdene er de rigtige, en håndholdt beholder med brændstof, der hældes i nærh
Video:Hvad er flammejetting?Kredit:The American Chemical Society Vi ved, at brændstoffer som benzin og alkohol kan brænde. Men nogle gange, når forholdene er de rigtige, en håndholdt beholder med brændstof, der hældes i nærh -
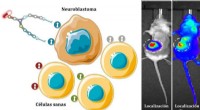 Syntetiske molekyler leverer lægemidler direkte til neuroblastomcellerKredit:Angewandte Chemie-International Edition 58 (2019) Forskere fra Universidad Politécnica de Madrid er involveret i udviklingen af specifikke molekylære stilladser, som er i stand til at lev
Syntetiske molekyler leverer lægemidler direkte til neuroblastomcellerKredit:Angewandte Chemie-International Edition 58 (2019) Forskere fra Universidad Politécnica de Madrid er involveret i udviklingen af specifikke molekylære stilladser, som er i stand til at lev -
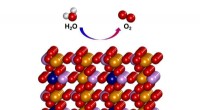 Elektrokatalysator udviser fremragende vandspaltningsaktivitetVist ovenfor demonstrerer den teoretisk forudsagte struktur af Fe 3 Co(PO 4 ) 4 @rGO. Jern (Fe) er angivet som gul, kobolt (Co) i blåt, fosforsyre (P) i lilla, oxygen (O) i rødt, og hydrogen (H)
Elektrokatalysator udviser fremragende vandspaltningsaktivitetVist ovenfor demonstrerer den teoretisk forudsagte struktur af Fe 3 Co(PO 4 ) 4 @rGO. Jern (Fe) er angivet som gul, kobolt (Co) i blåt, fosforsyre (P) i lilla, oxygen (O) i rødt, og hydrogen (H)
- Er det trie eller falsk, at alle elektromagnetiske bølger bevæger sig med samme hastighed i et vak…
- Er et navn lav skyer er tåge?
- Hvad er den enkleste form for celleorganisation?
- Kina fabrikker rationerer strøm, da hedebølgen sender efterspørgslen i vejret
- Hvad er det sted, hvor Glacier stoppede med at bevæge sig og faldt klipper snavs, det bar, kaldet?
- Proteinsyntese:En omfattende guide til transkription og oversættelse


