Forståelse af hydroxidiondannelse:En detaljeret forklaring
Sådan sker det:
* Vand er et polært molekyle: Det betyder, at oxygenatomet har en svagt negativ ladning, mens brintatomerne har en svagt positiv ladning.
* Selvionisering: Vandmolekyler kan interagere med hinanden. Nogle gange overføres en hydrogenion (H+) fra et vandmolekyle til et andet.
* Danning af ioner: Vandmolekylet, der mister en brintion, bliver til en hydroxidion (OH-), mens det vandmolekyle, der får brintionen, bliver til en hydroniumion (H3O+).
Her er en forenklet fremstilling:
H2O + H2O ⇌ H3O+ + OH-
Denne reaktion er reversibel , hvilket betyder, at det kan gå i begge retninger. Men i rent vand er koncentrationen af både hydroxidioner og hydroniumioner meget lille, hvilket resulterer i en neutral pH.
Nøgleafhentning: Vands evne til at ionisere er afgørende for mange kemiske reaktioner, og dannelsen af hydroxidioner er en nøglefaktor for at bestemme pH i en opløsning.
 Varme artikler
Varme artikler
-
 Mestring af molforhold:Fra empiriske formler til afbalancerede ligningerAf Chris Deziel | Opdateret 24. marts 2022 Inden for støkiometriens område - hvor kemikere sammenligner de relative mængder af stoffer i reaktioner - er det vigtigt at vide, hvordan man bestemmer mol
Mestring af molforhold:Fra empiriske formler til afbalancerede ligningerAf Chris Deziel | Opdateret 24. marts 2022 Inden for støkiometriens område - hvor kemikere sammenligner de relative mængder af stoffer i reaktioner - er det vigtigt at vide, hvordan man bestemmer mol -
 Nyt reaktor-foringslegeringsmateriale giver styrke, modstandsdygtighedOsman El Atwani (til venstre) og Enrique Martinez ved transmissionselektronmikroskopet. Kredit:Los Alamos National Laboratory En ny wolfram-baseret legering udviklet ved Los Alamos National Labora
Nyt reaktor-foringslegeringsmateriale giver styrke, modstandsdygtighedOsman El Atwani (til venstre) og Enrique Martinez ved transmissionselektronmikroskopet. Kredit:Los Alamos National Laboratory En ny wolfram-baseret legering udviklet ved Los Alamos National Labora -
 Saccharose:Forstå hvorfor det er et ikke-reducerende sukker | Kemi forklaretAf Claire Gillespie Opdateret 24. marts 2022 Håndlavede billeder/iStock/GettyImages Du kan bruge sukker på daglig basis ved at tilføje det til dine opskrifter og varme drikke for at gøre dem sødere
Saccharose:Forstå hvorfor det er et ikke-reducerende sukker | Kemi forklaretAf Claire Gillespie Opdateret 24. marts 2022 Håndlavede billeder/iStock/GettyImages Du kan bruge sukker på daglig basis ved at tilføje det til dine opskrifter og varme drikke for at gøre dem sødere -
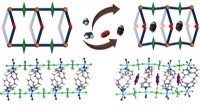 Absorberet pasform til acetylenKredit:Wiley Vi siger ofte, at et substrat passer ind i sit enzym som en nøgle i en lås, men denne metafor er ufuldkommen. Substratbinding kan også ændre låsen (enzymets struktur) for at fremkalde
Absorberet pasform til acetylenKredit:Wiley Vi siger ofte, at et substrat passer ind i sit enzym som en nøgle i en lås, men denne metafor er ufuldkommen. Substratbinding kan også ændre låsen (enzymets struktur) for at fremkalde
- Ny konkurrence om MOF'er:Forskere laver stærkere COF'er
- Microgel-pulver bekæmper infektioner og hjælper med at hele sår
- Hvordan kreditplatforme kan gøre banklånslofter ineffektive
- Hvordan fungerer en elektromagnet i en højttaler?
- Huawei flytter forskning fra fjendtlige USA til Canada:grundlægger
- Hvad er menneskelige spiser?


