Monomer vs. Polymer:Forståelse af kemiske egenskabsforskelle
* Struktur: Monomerer er enkelte, simple molekyler, mens polymerer er store kæder bygget af mange gentagne monomerenheder. Denne forskel i struktur påvirker markant, hvordan molekylerne interagerer med hinanden og med andre stoffer.
* Intermolekylære kræfter: Polymerer har mange flere muligheder for intermolekylære kræfter (som hydrogenbinding eller van der Waals-kræfter) end monomerer. Disse kræfter påvirker egenskaber som smeltepunkt, kogepunkt, opløselighed og fleksibilitet.
* Funktionelle grupper: Måden funktionelle grupper er arrangeret i en polymer kan være meget forskellig fra hvordan de er arrangeret i en monomer. Dette kan dramatisk ændre reaktivitet og kemisk adfærd.
Eksempler:
* Ethylen (monomer) vs. polyethylen (polymer): Ethylen er en gas ved stuetemperatur, mens polyethylen er et fast stof. Ethylen er meget reaktivt, mens polyethylen er relativt inert.
* Glucose (monomer) vs. stivelse (polymer): Glukose er et simpelt sukker, der let opløses i vand. Stivelse er et komplekst kulhydrat, der er uopløseligt i vand.
Undtagelser:
Der er nogle undtagelser fra denne generelle regel. For eksempel kan nogle monomerer og polymerer dele nogle lignende egenskaber, såsom opløselighed i visse opløsningsmidler. Forskellene i overordnet kemisk adfærd er dog normalt signifikante.
Opsummering: Mens monomerer og polymerer er relateret til deres kemiske sammensætning, fører forskellene i deres struktur og størrelse til betydelige forskelle i deres kemiske egenskaber.
 Varme artikler
Varme artikler
-
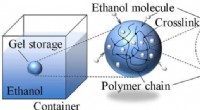 Forskere viser, hvordan man opbevarer flydende brændstoffer i polymere geler for at forhindre ekspl…Forskere fra SIT Japan viste i en ny undersøgelse, at kemisk tværbundne polymere gel-netværk kan fange meget flygtige flydende brændstofmolekyler, såsom ethanol, gennem fysiske interaktioner og derved
Forskere viser, hvordan man opbevarer flydende brændstoffer i polymere geler for at forhindre ekspl…Forskere fra SIT Japan viste i en ny undersøgelse, at kemisk tværbundne polymere gel-netværk kan fange meget flygtige flydende brændstofmolekyler, såsom ethanol, gennem fysiske interaktioner og derved -
 Revolutionær retsmedicinsk fingeraftryksteknik kan hjælpe med at bekæmpe bedrageriFingeraftrykket vil så fremstå enten maskeret (A), hvis det lægges ned før teksten blev trykt på papiret eller komplet (B), hvis det lægges ned efter at teksten var blevet udskrevet. Kredit:Loughborou
Revolutionær retsmedicinsk fingeraftryksteknik kan hjælpe med at bekæmpe bedrageriFingeraftrykket vil så fremstå enten maskeret (A), hvis det lægges ned før teksten blev trykt på papiret eller komplet (B), hvis det lægges ned efter at teksten var blevet udskrevet. Kredit:Loughborou -
 Afkobling af stress og korrosion for at forudsige metalfejlKredit:CC0 Public Domain Et forskningshold fra Arizona State University har frigivet ny indsigt om intergranular stress-corrosion cracking (SCC), en miljømæssig årsag til for tidlig fejl i konstru
Afkobling af stress og korrosion for at forudsige metalfejlKredit:CC0 Public Domain Et forskningshold fra Arizona State University har frigivet ny indsigt om intergranular stress-corrosion cracking (SCC), en miljømæssig årsag til for tidlig fejl i konstru -
 Ny højhastighedstest viser, hvordan antibiotika kombineres for at dræbe bakterierMed den modificerede agarplade CombiANT er det muligt at lave højhastighedstests for at se, hvordan bakterier reagerer på forskellige kombinationer af antibiotika. Kredit:Nikos Fatsis-Kavalopoulos
Ny højhastighedstest viser, hvordan antibiotika kombineres for at dræbe bakterierMed den modificerede agarplade CombiANT er det muligt at lave højhastighedstests for at se, hvordan bakterier reagerer på forskellige kombinationer af antibiotika. Kredit:Nikos Fatsis-Kavalopoulos
- Destillation af havvand er det fysisk eller kemisk ændring?
- Hvad er en måling, der inkluderer både hastighed og retning kaldet?
- Hvad er en faktor, der er nødvendig for dannelsen af nye arter?
- En styrke, der holder planeter i kredsløb?
- Krager kan bevidst planlægge, hvor mange opkald der skal foretages, viser undersøgelse
- ESA og NASA går sammen om at studere solvind


