Stærk syredissociation i vand:En omfattende forklaring
Det er vigtigt at bemærke, at udtrykket "helt" er lidt af en overforenkling. Teknisk set vil selv stærke syrer have en lille del af deres molekyler forblive udissocierede i opløsning. Denne fraktion er dog så lille, at vi af praktiske årsager anser stærke syrer for at være fuldstændigt dissocierede.
Her er en oversigt:
* Dissociation: Dette refererer til den proces, hvor et syremolekyle (som HCl) bryder fra hinanden i vand og danner ioner. I tilfælde af HCl danner det H+ (hydrogenion) og Cl- (chloridion).
* Stærke syrer: Det er syrer, der let donerer deres proton (H+) til vand, hvilket får opløsningen til at blive meget sur.
* Svage syrer: Disse syrer dissocierer kun delvist i vand, hvilket betyder, at de donerer en mindre del af deres protoner, hvilket resulterer i en mindre sur opløsning.
Eksempler på stærke syrer:
* Saltsyre (HCl)
* Salpetersyre (HNO3)
* Svovlsyre (H2SO4)
* Perchlorsyre (HClO4)
Husk: Den "næsten fuldstændig" dissociation af stærke syrer er en nøglefaktor i deres høje surhedsgrad og evnen til at lede elektricitet effektivt i opløsning.
 Varme artikler
Varme artikler
-
 Hvordan Jorden fanger solenergi:Videnskaben om planetarisk opvarmningAf David Sarokin Opdateret 24. marts 2022 Design Pics/Carl Shaneff/Design Pics/Getty Images Solen udstråler energi i alle retninger. Det meste af det spreder sig ud i rummet, men den lille del af s
Hvordan Jorden fanger solenergi:Videnskaben om planetarisk opvarmningAf David Sarokin Opdateret 24. marts 2022 Design Pics/Carl Shaneff/Design Pics/Getty Images Solen udstråler energi i alle retninger. Det meste af det spreder sig ud i rummet, men den lille del af s -
 Forskere håber, at en robo-næse kunne give K-9-officerer en pauseGolden retriever Rudy, iført militærhundeskilte og et amerikansk flag, bliver trænet af den amerikanske hær til at bruge sin fantastiske næse til at finde menneskelige rester. Kredit:Hærens foto H
Forskere håber, at en robo-næse kunne give K-9-officerer en pauseGolden retriever Rudy, iført militærhundeskilte og et amerikansk flag, bliver trænet af den amerikanske hær til at bruge sin fantastiske næse til at finde menneskelige rester. Kredit:Hærens foto H -
 Inde i brændselscellen:Imaging metode lover industriel indsigtHydrogenholdige stoffer er vigtige for mange industrier, men forskere har kæmpet for at få detaljerede billeder for at forstå elementets adfærd. I gennemgang af videnskabelige instrumenter, forskere d
Inde i brændselscellen:Imaging metode lover industriel indsigtHydrogenholdige stoffer er vigtige for mange industrier, men forskere har kæmpet for at få detaljerede billeder for at forstå elementets adfærd. I gennemgang af videnskabelige instrumenter, forskere d -
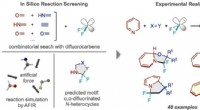 Simuleringer giver kort til skattekammeret af fluorerede forbindelserWorkflow af reaktionsopdagelse via in silico screening. (Venstre) Reaktioner mellem difluorcarben og adskillige par af små molekyler blev simuleret, hvilket forudsagde et N-heterocyklisk produkt fluor
Simuleringer giver kort til skattekammeret af fluorerede forbindelserWorkflow af reaktionsopdagelse via in silico screening. (Venstre) Reaktioner mellem difluorcarben og adskillige par af små molekyler blev simuleret, hvilket forudsagde et N-heterocyklisk produkt fluor
- Sammenlignet med en kold væske, hvordan ville partiklerne i varme væsker bevæge sig?
- Spinler cykloner modsat under ækvator?
- Russiske forskere udvikler et smart sorbent til vandrensning
- Forstå hvad der sker inde i flydende dråber
- Hvor ofte kan den mørke side af månen ses fra Jorden?
- Forskere producerer højstyrkepuds udelukkende af affald


