Kemiske reaktioner og massebevarelse:Forståelse af vægtændringer
Her er grunden til, at du måske *tror*, at et stof har mindre masse:
* Gasproduktion: En kemisk reaktion kan producere en gas, der slipper ud i atmosfæren. Dette tab af gas får det til at *vise* som om stoffet har mistet masse, men gassen er stadig til stede, bare ikke i beholderen.
* Fordampning eller sublimering: Hvis en væske eller et fast stof fordamper eller sublimerer (forvandles direkte til en gas), kan det virke som om, at massen går tabt. Imidlertid er det fordampede eller sublimerede materiale stadig til stede i luften som en gas.
* Ufuldstændige målinger: Nogle gange er måleteknikker måske ikke præcise nok til at tage højde for al den masse, der er involveret i en reaktion. Dette kan skabe illusionen om massetab.
Opsummeret, selvom det kan se ud til, at masse går tabt under en kemisk reaktion, forbliver systemets samlede masse konstant. Det er bare, at noget af massen kan være i en anden form eller placering, end den var oprindeligt.
Sidste artikelSvovlsyres rolle i alkoholoxidation med kaliumdichromat
Næste artikelJernfosfat kemisk formel (Fe3(PO4)2) Forklaret
 Varme artikler
Varme artikler
-
 Forskere skaber nyt byggemateriale af svamp, ris og glasSvampestensprototyper fremstillet af risskaller og affald af glasaffald. Kredit:Tien Huynh, Forfatter angivet Ville du bo i et hus lavet af svamp? Det er ikke kun et retorisk spørgsmål:svampe er n
Forskere skaber nyt byggemateriale af svamp, ris og glasSvampestensprototyper fremstillet af risskaller og affald af glasaffald. Kredit:Tien Huynh, Forfatter angivet Ville du bo i et hus lavet af svamp? Det er ikke kun et retorisk spørgsmål:svampe er n -
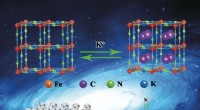 Direkte konvertering af rustent rustfrit stålnet til stabilt, billige elektroder til kalium-ion-bat…Kinesiske videnskabsmænd har gjort god brug af affald, mens de har fundet en innovativ løsning på et teknisk problem ved at omdanne rustent rustfrit stålnet til elektroder med fremragende elektrokemis
Direkte konvertering af rustent rustfrit stålnet til stabilt, billige elektroder til kalium-ion-bat…Kinesiske videnskabsmænd har gjort god brug af affald, mens de har fundet en innovativ løsning på et teknisk problem ved at omdanne rustent rustfrit stålnet til elektroder med fremragende elektrokemis -
 Forskere finder bisulfater, der begrænser effektiviteten af dieselmotorkatalysatorerKredit:CC0 Public Domain Et team af forskere fra Yale-NUS College, i samarbejde med forskere i Sverige, har fundet ud af, at bisulfatarter i udstødningsstrømmen er stærkt forbundet med at forminds
Forskere finder bisulfater, der begrænser effektiviteten af dieselmotorkatalysatorerKredit:CC0 Public Domain Et team af forskere fra Yale-NUS College, i samarbejde med forskere i Sverige, har fundet ud af, at bisulfatarter i udstødningsstrømmen er stærkt forbundet med at forminds -
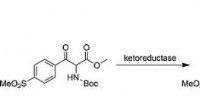 Syntese af det veterinære antibiotikum florfenicol ad en hurtig kemo-enzymatisk vejKredit: European Journal of Organic Chemistry Fluorerede strukturer udgør mere end 20 procent af moderne lægemidler, men godartede og hurtige fluoreringsskemaer er knappe. I en undersøgelse offen
Syntese af det veterinære antibiotikum florfenicol ad en hurtig kemo-enzymatisk vejKredit: European Journal of Organic Chemistry Fluorerede strukturer udgør mere end 20 procent af moderne lægemidler, men godartede og hurtige fluoreringsskemaer er knappe. I en undersøgelse offen
- Hvilket år blev konstellationskræft fundet?
- Hvordan jagt kan have forvandlet mennesker til langdistanceløbere
- Hvad er eksempler på kul og benzin?
- Hvad er forskellen mellem en græsareal og våd græsareal?
- Hvorfor er det vigtigt oto sperter elektricitet?
- Mikroplastik kommer alle vegne fra – ja, det inkluderer sexlegetøj


