Svovlsyres rolle i alkoholoxidation med kaliumdichromat
Hvorfor K₂Cr₂O₇ alene ikke er nok
* K₂Cr₂O₇ som et oxidationsmiddel: Kaliumdichromat er et kraftigt oxidationsmiddel, hvilket betyder, at det let accepterer elektroner. Denne egenskab gør det muligt for den at oxidere alkoholer.
* Kromationer er de aktive arter: Oxidationsmidlet i denne reaktion er chromationen (CrO4²⁻), som dannes, når K2Cr2O7 opløses i vand.
* Behovet for syre: Kromationen er mest effektiv som oxidationsmiddel i sure opløsninger. H2SO4 giver det sure miljø.
Hvordan H₂SO₄ spiller en nøglerolle
1. Protonation: H₂SO4 protonerer alkoholen, hvilket gør den mere modtagelig for oxidation. Dette sker gennem dannelsen af en protoneret alkohol, som er en bedre elektrofil (mere tilbøjelig til at acceptere elektroner).
2. Danning af kromsyre: Den vigtigste rolle for H₂SO4 er at reagere med kromationen (CrO₄²⁻) for at danne chromsyre (H₂CrO₄) . Denne reaktion er en ligevægt, men tilstedeværelsen af syre skubber ligevægten mod dannelse af kromsyre.
3. Kromsyre som den aktive oxidant: Chromsyre er det sande oxidationsmiddel i denne reaktion. Det reagerer med den protonerede alkohol og danner det oxiderede produkt (aldehyd eller keton).
Den kemiske ligning
En forenklet fremstilling af den overordnede reaktion er:
3RCH2OH + K2Cr2O7 + 4H2SO4 → 3RCHO + K2SO4 + Cr2(SO4)3 + 7H2O
Nøglepunkter
* Syrestyrke: Stærke syrer som H2SO4 foretrækkes, fordi de sikrer en tilstrækkelig koncentration af H+-ioner i opløsningen.
* Kromsyres farve: Opløsningen ændrer farve under reaktionen, ofte fra orange til grøn, på grund af reduktionen af kromationer til Cr³⁺-ioner.
* Reaktionsbetingelser: Reaktionen udføres typisk ved forhøjede temperaturer for at accelerere oxidationsprocessen.
Sig til, hvis du vil have en mere detaljeret forklaring på nogle af disse punkter!
 Varme artikler
Varme artikler
-
 Superhurtig indsigt i mobilbegivenhederFrankfurt-forskere fulgte bevægelserne af dette lille molekyle - kun to tusindedele af tykkelsen af et stykke papir. RNA-aptameren ændrer sin struktur, når den binder hypoxanthin. De grønne nukleoba
Superhurtig indsigt i mobilbegivenhederFrankfurt-forskere fulgte bevægelserne af dette lille molekyle - kun to tusindedele af tykkelsen af et stykke papir. RNA-aptameren ændrer sin struktur, når den binder hypoxanthin. De grønne nukleoba -
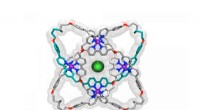 Molekylær knude vinder rekord for verdens strammesteRøntgenkrystalstruktur af en molekylær knude med otte krydsninger. Kredit:Jean-Francois Lemonnier, University of Manchester Forskere ved University of Manchester fejrer efter at være blevet rekord
Molekylær knude vinder rekord for verdens strammesteRøntgenkrystalstruktur af en molekylær knude med otte krydsninger. Kredit:Jean-Francois Lemonnier, University of Manchester Forskere ved University of Manchester fejrer efter at være blevet rekord -
 Bliver ung, fra cellerne og opKredit:CC0 Public Domain Forskere ved Université de Montréal og McGill University har opdaget et nyt multi-enzymkompleks, der omprogrammerer stofskiftet og overvinder cellulær senescens, når aldr
Bliver ung, fra cellerne og opKredit:CC0 Public Domain Forskere ved Université de Montréal og McGill University har opdaget et nyt multi-enzymkompleks, der omprogrammerer stofskiftet og overvinder cellulær senescens, når aldr -
 Upcycling svampet plastikskum fra sko, madrasser og isoleringPolyurethanskum er notorisk vanskelige at genbruge og ender på lossepladser eller i produkter med lavere værdi, såsom syntetiske tæpper. Kredit:Northwestern University Forskere har udviklet en ny
Upcycling svampet plastikskum fra sko, madrasser og isoleringPolyurethanskum er notorisk vanskelige at genbruge og ender på lossepladser eller i produkter med lavere værdi, såsom syntetiske tæpper. Kredit:Northwestern University Forskere har udviklet en ny
- Vil afbalancerede kræfter på AB -objekt ændre sin bevægelse?
- Hvornår blev det mørke feltmikroskop opfundet?
- Fjernpulssensorer kan være forspændt mod mørkere hud. UCLA-teamet tilbyder løsning
- Hvilket navn på et sted, der bruger teleskoper og andet videnskabeligt udstyr til at forskningsrum …
- Bindingerne mellem fosfatgrupperne i ATP har store mængder kemisk?
- Verdens luftfartsselskaber forpligter sig til netto nul CO2-emissioner inden 2050


