Hvordan rekombinant DNA-teknologi transformerede menneskers sundhed, landbrug og miljø
Supapich Methaset/Shutterstock
Forskere søger konstant måder at forbedre menneskets velbefindende på, og rekombinant DNA (rDNA) er et stærkt værktøj i denne søgen. Selvom rDNA tilbyder bemærkelsesværdige fordele, rejser det også etiske spørgsmål – især omkring den bevidste sammensmeltning af genetisk materiale fra forskellige arter – og bekymringer om utilsigtede miljøpåvirkninger. At forstå teknologiens fordele kræver en klar forståelse af, hvordan rDNA er opbygget.
Gennembruddet kom i 1968 med opdagelsen af restriktionsenzymer - bakterielle proteiner, der skærer fremmed DNA på præcise steder for at neutralisere patogener. I 1973 samlede forskerne med succes de første rekombinante DNA-molekyler, en proces, der involverer isolering af DNA, udskæring af et fragment på et specifikt locus, indsættelse af et nyt segment og derefter indføring af hybriden i en værtscelle, hvor den replikerer. Det indsatte fragment kan stamme fra enhver eukaryotisk organisme, hvad enten det er bakteriel, svampe, pattedyr eller menneskelig.
Splejsning af DNA på denne måde gør det muligt for forskere at klone sunde celler til terapeutisk erstatning eller at give værtsceller nye egenskaber, såsom toksinproduktion eller lægemiddelresistens. På grund af dets alsidighed har rDNA omformet medicin, landbrug og miljøforvaltning.
Behandling og helbredelse af sygdomme
zoehaswitt/Shutterstock
Inden for medicin er rDNA's mest berømte bidrag i genterapi, som korrigerer arvelige mutationer, der forårsager et spektrum af genetiske lidelser. Det understøtter også produktionen af livreddende proteiner – især insulin til diabetes, rekombinant humant væksthormon til hypofysemangler og koagulationsfaktorer til blødningsforstyrrelser.
Før 1982 blev insulin udvundet fra bugspytkirtlen fra kvæg eller svin, en kilde, der kan udløse allergiske reaktioner hos nogle patienter. Det første rekombinante insulin, Humulin, blev godkendt af FDA det år, hvilket markerede debuten for et moderne biologisk lægemiddel. Humulin er udviklet af Lilly og Genentech og er fortsat en hjørnesten i diabetesbehandling.
Rekombinant væksthormonbehandling erstatter det hormon, som en defekt hypofyse ikke formår at producere, hvilket gør det muligt for børn med væksthormonmangel at nå deres genetiske højdepotentiale.
Forebyggelse af spredning af sygdomme og vira
Peopleimages/Getty Images
Vacciner beskytter ikke kun enkeltpersoner, men hele samfund. rDNA-teknologi revolutionerede vaccineudviklingen, begyndende med hepatitis B-vaccinen i 1986. Ved at udtrykke hepatitis B-overfladeantigenet (HBsAg) i gær- eller pattedyrsceller kan producenter producere en praktisk talt ubegrænset forsyning af et protein, der efterligner den naturlige virale overflade. Vacciner som Engerix-B og Recombivax-HB er fortsat de mest udbredte på verdensplan og beskytter anslået 296 millioner bærere mod infektion.
Selvom rDNA-baserede vacciner stadig er sjældne, var de medvirkende til at producere Oxford-AstraZeneca COVID-19-vaccinen og Flublok-influenzavaccinerne, som helt undgår hønseæg og viruskulturer. Flublok Quadrivalent, godkendt i 2016, er særligt effektiv til personer over 65 år, og tilbyder overlegen beskyttelse sammenlignet med konventionelle influenza-indsprøjtninger.
Forbedring af landbrug og afgrøder
Hryshchyshen Serhii/Shutterstock
Ud over sundhed styrker rDNA landbruget ved at indsætte specifikke DNA-segmenter i afgrødens genomer, hvilket skaber genetisk modificerede organismer, der har forbedrede egenskaber. Den første genmodificerede tomat, udgivet i 1994, blev udviklet til forsinket modning og forbedret smag. I dag produceres 88 % af amerikansk majs og 93 % af sojabønner gennem rDNA-baserede teknikker.
Mål for landbrugs-rDNA inkluderer at øge udbyttet pr. plante, øge modstandsdygtigheden over for skadedyr, styrke frøs levedygtighed og udvide afgrødestørrelsen. For eksempel udtrykker Bt-majs et Bacillus thuringiensis-toksin, der afskrækker visse insekter, hvilket reducerer afhængigheden af kemiske pesticider. Gyldne ris, beriget med β‑caroten, bekæmper A-vitaminmangel i sårbare befolkningsgrupper. Herbicid-tolerante sorter, såsom Roundup-Ready majs og soja, giver landmændene mulighed for at håndtere ukrudt uden at skade deres afgrøder.
Forbedring af konservering og fremstilling af fødevarer
PanuShot/Shutterstock
Rekombinante enzymer strømliner fødevareforarbejdning og konservering. Amylaser, serinproteaser og glucoseoxidase produceret via rDNA hæmmer ødelæggende mikrober og forbedrer produktkvaliteten. I fødevareindustrien letter disse enzymer omdannelsen af stivelse til sukker til majssirupproduktion med høj fructose, hvilket øger effektiviteten og smagen.
Ostefremstilling drager også fordel af rekombinant chymosin, et rennin-enzym, der traditionelt høstes fra kalvemaver. Siden 1990 har mikrober udviklet til at producere ren rekombinant chymosin muliggjort storskala, vegetarvenlig osteproduktion, hvilket eliminerer behovet for animalske enzymkilder.
Løsning af jord- og vandforureningsproblemer
I.NoyanYilmaz/Shutterstock
rDNA er også afgørende i bioremediering, hvor konstruerede mikrober - bakterier, svampe eller gær - er skræddersyet til at nedbryde farlige forurenende stoffer. Genetisk modificerede E.coli og Pseudomonas putida kan for eksempel omsætte genstridige forurenende stoffer i spildevand, mens manipulerede stammer er målrettet mod tungmetaller som kviksølv og nikkel i jord og vand. Ved hurtigt at tilpasse sig nye forurenende stoffer tilbyder disse GEM'er en omkostningseffektiv og kraftfuld løsning til beskyttelse af miljø og menneskers sundhed.
 Varme artikler
Varme artikler
-
 Pigmenternes afgørende rolle i fotosyntesenHvad er fotosyntese? Fotosyntese er den naturlige proces, hvorved lysenergi omdannes til kemisk energi, der danner grundlaget for livet på Jorden. I denne proces absorberes fotoner af specialiserede
Pigmenternes afgørende rolle i fotosyntesenHvad er fotosyntese? Fotosyntese er den naturlige proces, hvorved lysenergi omdannes til kemisk energi, der danner grundlaget for livet på Jorden. I denne proces absorberes fotoner af specialiserede -
 Demonstrer bevarelse af masse:smeltende is-eksperimentAf Jaime Swanson | Opdateret 24. marts 2022 Comstock/Comstock/Getty Images Loven om bevarelse af masse siger, at den samlede masse af reaktanter og produkter forbliver konstant under en kemisk proce
Demonstrer bevarelse af masse:smeltende is-eksperimentAf Jaime Swanson | Opdateret 24. marts 2022 Comstock/Comstock/Getty Images Loven om bevarelse af masse siger, at den samlede masse af reaktanter og produkter forbliver konstant under en kemisk proce -
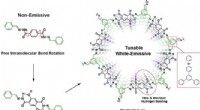 Justerbar emissiv organisk platformFigur viser designprincipperne for udvikling af en justerbar 2D COF, der er i stand til at udsende hvidt lys. Den frie intramolekylære bindingsrotation gør den grundlæggende molekylære enhed ikke-emit
Justerbar emissiv organisk platformFigur viser designprincipperne for udvikling af en justerbar 2D COF, der er i stand til at udsende hvidt lys. Den frie intramolekylære bindingsrotation gør den grundlæggende molekylære enhed ikke-emit -
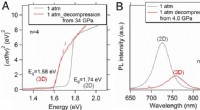 Trykinduceret 2D-3D konvertering i hybrid blyiodid lagdelt perovskit2D-3D overgang i hybrid perovskites. Kredit:Gang Liu Hydrostatisk tryk kan føre til nye og forbedrede materialeegenskaber. Imidlertid, de fleste nye materialeegenskaber kan kun bevares ved højtryk
Trykinduceret 2D-3D konvertering i hybrid blyiodid lagdelt perovskit2D-3D overgang i hybrid perovskites. Kredit:Gang Liu Hydrostatisk tryk kan føre til nye og forbedrede materialeegenskaber. Imidlertid, de fleste nye materialeegenskaber kan kun bevares ved højtryk
- Bestem ændringen i volumen, der finder sted, når 1,95-L prøve af N2g opvarmes fra 250,0 K til 442…
- Myrer i Ohio
- Forbedring af observation af proteinbinding
- Hvad er syrefældningen et middel for?
- Hvor højt over havets overflade er jeg? stiller det forkerte spørgsmål
- Et probiotikum for vores lunger? Ny forskning stiller spørgsmål om fremtiden for behandling af COV…


