Hvad driver kemiske reaktioner? Nøglefaktorer forklaret
Af John Brennan
Opdateret 30. august 2022
Kemiske reaktioner opstår, når to eller flere stoffer kolliderer og omarrangeres for at danne nye forbindelser. Disse processer er ikke kun allestedsnærværende i naturen, men understøtter også ethvert levende system - NASA definerer endda livet som et selvopretholdende kemisk system, der er i stand til darwinistisk evolution. Forståelse af de kræfter, der styrer, om en reaktion vil opstå – og hvor hurtigt – kræver et kig på tre kernebegreber:kollisioner, entropi og ligevægt.
Kollisioner:Det første skridt til forandring
For at en kemisk transformation kan begynde, skal molekyler mødes med den korrekte orientering og nok kinetisk energi til at bryde eksisterende bindinger. Ikke ethvert møde fører til en reaktion; reaktanterne skal kunne rekombinere til mere stabile produkter. For eksempel er heliumatomer kemisk inerte, fordi deres ydre elektronskal er komplet, så de danner sjældent nye bindinger med andre gasser. I modsætning hertil, når atomer har uparrede elektroner eller ufuldstændige skaller, kan de dele eller overføre elektroner, hvilket tillader bindinger at danne og frigive energi.
Termodynamik lader os forudsige, om en reaktion vil være gunstig:Hvis den nye forbindelses samlede energi er lavere end de enkelte reaktanters, er det resulterende molekyle stabilt, og reaktionen er energisk nedadgående.
Entropi:The Drive Toward Disorder
Entropi måler graden af tilfældighed eller uorden i et system. Termodynamikkens anden lov siger, at entropien i et lukket system aldrig kan falde. En reaktion, der øger den kombinerede entropi af systemet og dets omgivelser, er spontan. Når en reaktion ikke er spontan – såsom biosyntesen af proteiner – kobler organismer den til en energigenererende proces som glukosemetabolisme, som frigiver en stor mængde entropi og driver den overordnede proces fremad.
Fordi total entropi er svær at kvantificere direkte, bruger kemikere Gibbs frie energi (ΔG) til at vurdere spontanitet. Formlen ΔG =ΔH – TAS sammenligner entalpiændringen (ΔH) med temperaturen (T) gange entropiændringen (ΔS). En negativ ΔG indikerer, at en reaktion kan opstå spontant under de givne betingelser.
Ligevægt:Når frem og tilbage mødes
Selv en spontan reaktion kan være langsom; omdannelsen af kulstofatomer i diamant er for eksempel kemisk gunstig, men forløber over geologiske tidsskalaer. Desuden når mange reaktioner en dynamisk ligevægt, hvor fremadgående og omvendte hastigheder balancerer, hvilket ikke efterlader nogen nettoændring i koncentrationer af reaktanter eller produkter. Hvorvidt en reaktion fortsætter til fuldførelse, går i stå eller vender tilbage, afhænger af kinetiske barrierer, termodynamisk favorabilitet og de tilstedeværende specifikke forhold.
Ved at undersøge kollisioner, entropi og ligevægt sammen kan videnskabsmænd forudsige ikke kun, om en reaktion vil ske, men også hvor hurtigt den vil ske, og under hvilke omstændigheder den vil producere et bestemt produkt.
Referencer
- Peter Atkins &Loretta Jones, Chemical Principles, The Quest for Insight (4. udgave), 2008.
 Varme artikler
Varme artikler
-
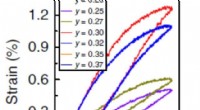 Nyt keramisk materiale kan reducere omkostningerne til piezoelektriske enhederKredit:Indian Institute of Science 1 procent), som er en markering af, hvor meget materialet kan ændre sin form, når det elektriske felt påføres. Imidlertid, de er meget dyre og svære at fremstill
Nyt keramisk materiale kan reducere omkostningerne til piezoelektriske enhederKredit:Indian Institute of Science 1 procent), som er en markering af, hvor meget materialet kan ændre sin form, når det elektriske felt påføres. Imidlertid, de er meget dyre og svære at fremstill -
 Forskning kan dramatisk sænke omkostningerne ved elektronkilderKunstnerens repræsentation af en halogenid perovskit fotokatode. Forskere ved Rice University og Los Alamos National Laboratory fandt, at halogenid-perovskit-halvledere (sølv) behandlet med et tyndt l
Forskning kan dramatisk sænke omkostningerne ved elektronkilderKunstnerens repræsentation af en halogenid perovskit fotokatode. Forskere ved Rice University og Los Alamos National Laboratory fandt, at halogenid-perovskit-halvledere (sølv) behandlet med et tyndt l -
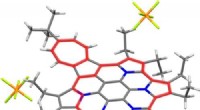 Dobbelt aromatiske ringe stabiliserer multikationerPyrrol- og azulenfusioneret azacoronen-dikering med 22π 6π aromatiske ringe. Kredit:American Chemical Society Et redoxaktivt polycyklisk aromatisk kulbrinte (PAHer) sammensat af azulen og pyrroler
Dobbelt aromatiske ringe stabiliserer multikationerPyrrol- og azulenfusioneret azacoronen-dikering med 22π 6π aromatiske ringe. Kredit:American Chemical Society Et redoxaktivt polycyklisk aromatisk kulbrinte (PAHer) sammensat af azulen og pyrroler -
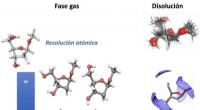 DNA -sukker karakteriseret i en hidtil uset opløsning, atom for atomTil venstre, strukturerne er fuldstændigt isoleret fra ethvert eksternt middel (opløsningsmiddel, krystallinsk bundtning) og til højre, strukturerne i vandet. I den mest rigelige struktur, de faste pr
DNA -sukker karakteriseret i en hidtil uset opløsning, atom for atomTil venstre, strukturerne er fuldstændigt isoleret fra ethvert eksternt middel (opløsningsmiddel, krystallinsk bundtning) og til højre, strukturerne i vandet. I den mest rigelige struktur, de faste pr
- Hvad påvirker elektromagnetisk kraft?
- Hvad er nukleotidsegmenter af DNA -molekyler, der udgør gener og udtrykt i fænotypen en organisme?…
- Forskning zoomer ind på enzym, der reparerer DNA-skader fra UV-stråler
- Hvad vi gør - og ikke ved om Pentagons hemmelige ufo-program
- Alternative græsplæner viser potentiale til brug på golfbaners fairways
- Hvilken kraft frembringer acceleration?


