Beregning af ligevægtskonstanten (Kc):En trin-for-trin guide
Af Bidragyder | Opdateret Aug302022
Ligevægtskonstanten Kc kvantificerer forholdet mellem produktkoncentrationer og reaktantkoncentrationer for en reaktion udført i opløsning eller gasfase, hvor alle arter er udtrykt som molære koncentrationer. For den generiske reaktion A+B⇌AB er den defineret som
Kc =[AB]⁄([A][B])
Nedenfor gennemgår vi to praktiske eksempler:oxidationen af carbonmonoxid med nitrogenoxid og den termiske nedbrydning af bagepulver (natriumbicarbonat).
1. Oxidation af CO med NO
Overvej den homogene ligevægt:
CO+2NO⇌CO2 +N2 O
Givet følgende molære koncentrationer:
- [CO]=2,0 molL⁻¹
- [NO]=0,5 molL⁻¹
- [CO2 ]=1,2 molL⁻1
- [N2 O]=3,0 molL-1
Beregn nævneren først:
[CO]×[NO]²=2,0×(0,5)²=1,0mol³L⁻³
Beregn derefter tælleren:
[CO2 ]×[N2 O]=1,2 x 3,0=3,6 mol2L-2
Til sidst divideres tæller med nævner:
Kc =(3,6mol²L⁻²)⁄(1,0mol³L⁻³)=3,6mol⁻¹L⁻¹
2. Termisk nedbrydning af bagepulver
Denne heterogene ligevægt involverer fast natriumbicarbonat og gasformige produkter:
2NaHCO3 ⇌Na2 CO3 +CO2 +H2 O
Kun gasformige arter forekommer i Kc udtryk, fordi faste stoffer er udeladt. Med følgende koncentrationer:
- [CO2 ]=1,8 molL⁻1
- [H2 O]=1,5 molL-1
Beregn:
Kc =[CO2 ]×[H2 O]=1,8 x 1,5=2,7 mol2L-2
Disse trinvise beregninger illustrerer, hvordan man bestemmer Kc for både homogene og heterogene reaktioner.
 Varme artikler
Varme artikler
-
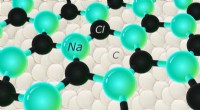 Salt værd:Forskere rapporterer det første tilfælde af sekskantet NaClKredit:Skolkovo Institut for Videnskab og Teknologi Skoltech- og MIPT-forskere har forudsagt og derefter eksperimentelt bekræftet eksistensen af eksotiske sekskantede tynde film af NaCl på en di
Salt værd:Forskere rapporterer det første tilfælde af sekskantet NaClKredit:Skolkovo Institut for Videnskab og Teknologi Skoltech- og MIPT-forskere har forudsagt og derefter eksperimentelt bekræftet eksistensen af eksotiske sekskantede tynde film af NaCl på en di -
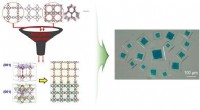 Algoritme identificerer optimale par til at sammensætte metal-organiske rammerFigur:Et eksempel på en rationelt syntetiseret MOF@MOFs (kubisk HKUST-1@MOF-5 ). Kredit:Korea Advanced Institute of Science and Technology (KAIST) Integrationen af metal-organiske rammer (MOFer
Algoritme identificerer optimale par til at sammensætte metal-organiske rammerFigur:Et eksempel på en rationelt syntetiseret MOF@MOFs (kubisk HKUST-1@MOF-5 ). Kredit:Korea Advanced Institute of Science and Technology (KAIST) Integrationen af metal-organiske rammer (MOFer -
 En ny katalysator til at bremse den globale opvarmningKredit:Shutterstock Russiske videnskabsmænd har udviklet en ny, højeffektiv katalysator til industriel forarbejdning af kuldioxid, der gør processen enkel og billig. Forskere fra MISIS University,
En ny katalysator til at bremse den globale opvarmningKredit:Shutterstock Russiske videnskabsmænd har udviklet en ny, højeffektiv katalysator til industriel forarbejdning af kuldioxid, der gør processen enkel og billig. Forskere fra MISIS University, -
 Genanvendelse af sjældne jordarters magneter er en kværn, men ny proces tager en enklere tilgangPlasma lommelygte afsætter genbrugsmagnetmateriale. Kredit:Ames Laboratory En ny genbrugsproces udviklet ved det amerikanske energiministeriums Critical Materials Institute (CMI) forvandler kasser
Genanvendelse af sjældne jordarters magneter er en kværn, men ny proces tager en enklere tilgangPlasma lommelygte afsætter genbrugsmagnetmateriale. Kredit:Ames Laboratory En ny genbrugsproces udviklet ved det amerikanske energiministeriums Critical Materials Institute (CMI) forvandler kasser


