Beregning af udbytte i procent:en trin-for-trin guide til reaktionseffektivitet
Af Ashley K. Ezell • Opdateret 30. august 2022
I laboratoriekemi kvantificerer det procentvise udbytte, hvor effektivt en reaktion producerer det ønskede produkt. Den sammenligner den faktiske masse af produktet opnået med det teoretiske maksimum forudsagt ved støkiometri, udtrykt som en procentdel.
Prøveudbytte
Forestil dig at nedsænke en 25-grams kobberprøve i en vandig sølvnitratopløsning - en klassisk fortrængningsreaktion, der skulle generere sølvmetal. Reaktionens støkiometri forudsiger et teoretisk udbytte på 85 g sølv. Efter filtrering og vejning vejer det genvundne sølv kun 82 g – dette er det faktiske udbytte.
Eksempelberegning
Procent udbytte beregnes med formlen:
Procentudbytte =(Faktisk udbytte ÷ Teoretisk udbytte) × 100
Anvendelse af tallene fra vores eksempel:82 g ÷ 85 g × 100 = 96 % Dette tal på 96 % indikerer, at reaktionen forløb med høj effektivitet; værdier tættere på 100 % afspejler færre bivirkninger, bedre oprensning og minimalt produkttab.
Hvorfor procent af udbytte betyder noget
Overvågning af procentudbytte hjælper kemikere:
- Identificer ineffektivitet eller urenheder i en procedure.
- Optimer reaktionsbetingelserne for at maksimere produktgenvinding.
- Benchmark reproducerbarhed på tværs af forskellige kørsler eller laboratorier.
Referencer
- Glencoe Chemistry:Matter and Change; Laurel Dingrando, et al.
Sidste artikelBeregning af molaritet ud fra molekylvægt:En trin-for-trin guide
Næste artikelFaktorer, der påvirker kemiresultater
 Varme artikler
Varme artikler
-
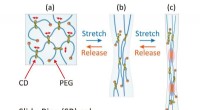 Biokompatible hydrogelmaterialer kan hurtigt komme sig efter mekanisk belastningEn strain gauge trækker prøver af hydrogel fra hinanden. (Øvre) En typisk gel med et hak skåret i venstre side snappede kort tid efter at den var strakt. (Midt) Den nye selvforstærkede gel havde et ha
Biokompatible hydrogelmaterialer kan hurtigt komme sig efter mekanisk belastningEn strain gauge trækker prøver af hydrogel fra hinanden. (Øvre) En typisk gel med et hak skåret i venstre side snappede kort tid efter at den var strakt. (Midt) Den nye selvforstærkede gel havde et ha -
 Mestring af Inconel Welding:Teknikker og bedste praksisInconel, en højtemperatur nikkel-chrom legering familie, er værdsat for sin exceptionelle korrosionsbestandighed og mekaniske styrke i krævende miljøer. Imidlertid gør dets legeringselementer det noto
Mestring af Inconel Welding:Teknikker og bedste praksisInconel, en højtemperatur nikkel-chrom legering familie, er værdsat for sin exceptionelle korrosionsbestandighed og mekaniske styrke i krævende miljøer. Imidlertid gør dets legeringselementer det noto -
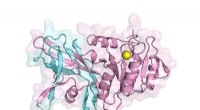 Forskere visualiserer strukturen af et nøgleenzym, der fremstiller triglyceriderEt første kig på strukturen af lipin-enzymet. Strukturen viser, hvordan to væsentlige områder (farvet blå og pink), placeret på modsatte ender af proteinet hos mennesker, samles for at danne et funk
Forskere visualiserer strukturen af et nøgleenzym, der fremstiller triglyceriderEt første kig på strukturen af lipin-enzymet. Strukturen viser, hvordan to væsentlige områder (farvet blå og pink), placeret på modsatte ender af proteinet hos mennesker, samles for at danne et funk -
 Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn:
Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn:
- Hvordan danner solenergi trin for trin?
- Hvad betyder jorden tilbage?
- Hvilke slags ændringer kan omdanne et depositum, der er en malm til ikke malm?
- Boeings bekymrede Starliner-kapselen, der nu sigter mod lanceringen i juli
- Højhastighedstog på Australiens østkyst vil øge emissionerne i op til 36 år
- Hvad sker der med termisk energi i et bæger, når det køles ned?


