Aluminiumskorrosion og kemiske transformationer:Forståelse af beskyttende oxidlag
Medioimages/Photodisc/Photodisc/Getty Images
Rent aluminium
Aluminium findes ikke naturligt i sin elementære form, fordi dets høje reaktivitet driver det til at kombinere med andre elementer. Det udvindes typisk fra malmen bauxit, som forarbejdes ved Bayer-metoden til fremstilling af aluminiumoxid (Al₂O₃). Den efterfølgende Hall-Héroult elektrolytiske reduktion omdanner aluminiumoxid til metallisk aluminium. Fordi aluminiumioner bærer en ladning på +3, bruger processen store mængder elektricitet for at tilføje de manglende elektroner.
Aluminiumoxid
Den kemiske formel for aluminiumoxid er Al2O3. I denne forbindelse balancerer to Al³⁺-ioner seks O²⁻-ioner, hvilket resulterer i et neutralt gitter. Når det udsættes for luft, reagerer rent aluminium med ilt og danner et tyndt, tæt lag af Al₂O3 på overfladen. Dette oxid er et hårdt krystallinsk materiale med et smeltepunkt på over 2.000°C (3.632°F), hvilket bidrager til dets beskyttende egenskaber.
Modstand mod korrosion
Dannelsen af oxidlaget er et klassisk eksempel på passivering:Metallet mister elektroner til oxygen, men det nydannede Al₂O3 hæfter kraftigt til overfladen og skærmer det underliggende metal mod yderligere angreb. Ved at anvende kontrolleret elektrolyse kan producenter bevidst fortykke denne oxidbarriere, hvilket øger korrosionsbestandigheden i krævende miljøer.
Ændring af oxidlaget
Aluminiumoxid er ikke kemisk inert. I alkaliske miljøer reagerer oxidet med hydroxidioner for at producere opløseligt aluminiumhydroxid, hvilket kompromitterer den beskyttende film og udsætter basismetallet for korrosion. Derfor er det tilrådeligt at undgå tilberedning af aluminium køkkengrej i basisfødevarer eller at bruge skrappe alkaliske rengøringsmidler. I modsætning hertil kan sure opløsninger faktisk forstærke oxidlaget, hvilket gør metallet mere modstandsdygtigt over for efterfølgende korrosion.
 Varme artikler
Varme artikler
-
 Ny kobberbelægning kunne blive den næste superbug fighterKredit:Pixabay/CC0 Public Domain En ny kobberbelægning, der dræber bakterier hurtigere og i større mængder end de nuværende formuleringer, kan snart være tilgængelig for hospitaler og andre højtraf
Ny kobberbelægning kunne blive den næste superbug fighterKredit:Pixabay/CC0 Public Domain En ny kobberbelægning, der dræber bakterier hurtigere og i større mængder end de nuværende formuleringer, kan snart være tilgængelig for hospitaler og andre højtraf -
 Eleven bruger planteaffald til at skabe et bæredygtigt alternativ til farvestofKredit:Imperial College London Kejserstuderende Nicole Stjernswärd bruger planteaffald til at skabe naturlige pulverpigmenter, der kan bruges til maling, blæk eller tekstiler. Historisk set kom f
Eleven bruger planteaffald til at skabe et bæredygtigt alternativ til farvestofKredit:Imperial College London Kejserstuderende Nicole Stjernswärd bruger planteaffald til at skabe naturlige pulverpigmenter, der kan bruges til maling, blæk eller tekstiler. Historisk set kom f -
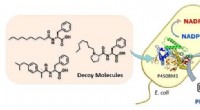 Tricker bakterier til hydroxylerende benzenFig.1 Phenolproduktion ved hjælp af bakterier. Kredit:Osami Shoji og Masayuki Karasawa Forskere ved Nagoya University bruger E.coli til at omdanne benzen til phenol, forenkling af en kemisk reakti
Tricker bakterier til hydroxylerende benzenFig.1 Phenolproduktion ved hjælp af bakterier. Kredit:Osami Shoji og Masayuki Karasawa Forskere ved Nagoya University bruger E.coli til at omdanne benzen til phenol, forenkling af en kemisk reakti -
 Forskere udvikler metode til at beregne transparente materialers porøsitetForskere fra Far Eastern Federal University (FEFU) har brugt en unik matematisk model til at beregne dataene for 3D-billeder af defekter i mængden af gennemsigtige funktionelle materialer. Det indle
Forskere udvikler metode til at beregne transparente materialers porøsitetForskere fra Far Eastern Federal University (FEFU) har brugt en unik matematisk model til at beregne dataene for 3D-billeder af defekter i mængden af gennemsigtige funktionelle materialer. Det indle
- Hvordan termisk energi når overfladen?
- Hvad resulterer hydrolysen af et neutralt fedt i?
- Hvis en klippe er begravet dybt inde i jorden, hvilken geologisk proces ikke kan ændre sten?
- Hvorfor er hvide dværge så tæt?
- Den bedste forklaring på, hvordan mennesker befolket jorden er?
- Hvorfor dannes huler undertiden på kysten?


