Sådan beregnes molaritet:En praktisk vejledning for kemikere
Ryan McVay/Photodisc/Getty Images
Uanset om du udfører et laboratorieeksperiment eller tager fat på en eksamen, er beregning af molaritet en grundlæggende færdighed i kemi. Molaritet kvantificerer, hvor koncentreret en opløsning er, udtrykt som antallet af mol opløst stof pr. liter opløsning. Beregningen kræver kun en simpel formel og nogle få nøgledata.
Forstå formlen
I sin mest basale form beregnes molaritet (M) ved at dividere antallet af mol opløst stof med opløsningens volumen i liter:
M =mol opløst stof ÷ liter opløsning
Dette forhold skrives ofte som "molL⁻¹" eller "mol per liter."
Find ud af muldvarpe
For at bestemme mol af et opløst stof har du brug for massen af det opløste stof, dets kemiske formel og atomvægtene af dets bestanddele (kan fås fra det periodiske system). Sum atomvægtene for at finde den molære masse, og divider derefter massen af det opløste stof med den molære masse.
Måling af løsningen
Opløsningens rumfang skal udtrykkes i liter for molaritetsformlen. Hvis volumen er angivet i milliliter, divideres med 1.000 for at omregne til liter.
Sæt det sammen
Eksempel:Opløs 20 g NaOH i 500 ml vand.
- Konverter volumen:500mL ÷ 1.000 =0,500L.
- Bestem molær masse af NaOH:Na(23g) + O(16g) + H(1g) =40gmol⁻¹.
- Beregn mol:20g ÷ 40gmol⁻¹ =0,500mol.
- Beregningsmolaritet:0,500mol ÷ 0,500L =1,0M.
Den resulterende opløsning har således en molaritet på 1 molL⁻1.
Gå videre
Når du mestrer den grundlæggende formel, kan du omarrangere den for at løse enhver ukendt - hvad enten det er mængden af opløst stof, antallet af mol eller volumenet af opløsning - ved hjælp af algebraisk manipulation. Denne fleksibilitet er afgørende for støkiometriske beregninger, titreringsanalyser og forberedelse af opløsninger med ønskede koncentrationer.
Sidste artikelAt lære børn om elektroner:En praktisk vejledning
Næste artikelForstå dieselbrændstof:typer, produktion og miljøpåvirkning
 Varme artikler
Varme artikler
-
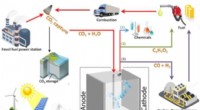 Forskere laver alkohol ud af den blå luftTre forskellige måder, hvorpå elektroreduktion af CO2 potentielt kan lukke kulstofkredsløbet. Kredit:Delft University of Technology Det lyder måske for godt til at være sandt, men TU Delft-ph.d.-s
Forskere laver alkohol ud af den blå luftTre forskellige måder, hvorpå elektroreduktion af CO2 potentielt kan lukke kulstofkredsløbet. Kredit:Delft University of Technology Det lyder måske for godt til at være sandt, men TU Delft-ph.d.-s -
 Ny teknologi muliggør hurtig proteinsynteseMIT-kemikere har udviklet en protokol til hurtigt at producere proteinkæder på op til 164 aminosyrer lange. Den flow-baserede teknologi kunne fremskynde udviklingen af lægemidler og give forskere mu
Ny teknologi muliggør hurtig proteinsynteseMIT-kemikere har udviklet en protokol til hurtigt at producere proteinkæder på op til 164 aminosyrer lange. Den flow-baserede teknologi kunne fremskynde udviklingen af lægemidler og give forskere mu -
 En laserdrevet programmerbar berøringsfri transfertrykteknik(A) Skematisk illustration af den laserdrevne programmerbare berøringsfri transfertrykproces via et aktivt elastomerisk mikrostruktureret stempel. (B) Udskrivning af enkelt Si-blodplade og LED-chip på
En laserdrevet programmerbar berøringsfri transfertrykteknik(A) Skematisk illustration af den laserdrevne programmerbare berøringsfri transfertrykproces via et aktivt elastomerisk mikrostruktureret stempel. (B) Udskrivning af enkelt Si-blodplade og LED-chip på -
 Hyperpolariseret proton -MR bruges til at observere metaboliske processer i realtidFantomet brugt til hyperpolariseret billeddannelse, med en illustration af billedskiver erhvervet ved hjælp af den nye teknik. Kredit:©:Laurynas Dagys, University of Southampton Magnetic resonance
Hyperpolariseret proton -MR bruges til at observere metaboliske processer i realtidFantomet brugt til hyperpolariseret billeddannelse, med en illustration af billedskiver erhvervet ved hjælp af den nye teknik. Kredit:©:Laurynas Dagys, University of Southampton Magnetic resonance
- Forståelse af pH og hydroniumioner (H3O+):En omfattende vejledning
- Hvilken gren af videnskaben hører meteorologi til?
- Regeringen, lærere og rektorer på vej i forskellige retninger om, hvorfor Asien-kompetence er vigt…
- Hvad sker der, når forurening kommer i jordens naturlige ressourcer?
- Hvad er fordele og ulemper ved energimåler?
- Hvad er korrosive materialer?


