Sådan skriver og afbalancerer du en kemisk formel:En trin-for-trin guide
Af Grahame Turner | Opdateret 30. august 2022
En kemisk formel er en kortfattet, standardiseret repræsentation af en kemisk reaktion. Selvom de kan virke skræmmende i starten, gør forståelsen af logikken bag hver komponent dem ligetil.
Trin 1 – Identificer reaktionskomponenterne
Start med den skriftlige reaktion. Se efter nøgleord som "brændt", "reagerer med" eller "giver sig". For eksempel, hvis teksten siger "methan (CH4 ) er brændt," du ved, at reaktanterne er CH4 og O2 (ilt). Produkterne vil følge ordet "udbytter."
Trin 2 – Skriv standardnotationen
Angiv hver art i dens kemiske formel:CH4 , O2 , CO2 , H2 O. Ordet "udbytter" angiver transformationen, så placer reaktanter på venstre side af pilen og produkter til højre.
Trin 3 – Konverter til en kemisk ligning
Erstat narrative verber med symboler:"giver" bliver til →, og adskil hver art med et plustegn (+). Tænk på hver formel som et særskilt molekyle. Til en brændende reaktion har du typisk brug for yderligere O2 for at matche støkiometrien.
Trin 4 – Balancer ligningen
Anvend loven om bevarelse af masse:atomer, der kommer ind i reaktionen, skal forlade i lige mange. Tæl atomerne af hvert grundstof på begge sider. Til metanforbrænding:CH4 + O2 → CO2 + H2 ODu finder fire hydrogenatomer til venstre, men kun to i H2 O til højre. Sæt en 2'er foran H2 O således at hver CH4 producerer to vandmolekyler.
Trin 5 – Juster ilt
Efter afbalancering af brint, kontroller ilt. Reaktionen har nu fire oxygenatomer i produkterne, men kun to i det enkelte O2 molekyle til venstre. Sæt en 2'er før O2 at levere de nødvendige atomer:CH4 + 2 O2 → CO2 + 2 H2 ODenne fuldt afbalancerede ligning opfylder nu bevaringsprincippet.
Trin 6 – Bekræft konservering
Bekræft, at hvert elements antal er identisk på begge sider. Husk, at en kemisk ligning ikke kan skabe eller ødelægge atomer; det omarrangerer dem kun.
TL;DR
Kemiske ligninger er typisk udtrykt i mol, men balancering kan visualiseres med individuelle molekyler. En muldvarp er lig med 6,0221415×10 23 entiteter – brug dette som reference, når du kontrollerer støkiometri.
 Varme artikler
Varme artikler
-
 Fluorescerende teknik bringer ældningspolymerer frem i lysetOpvarmning af et tyndt stykke polypropylen i 30-150 minutter forårsager ældning, som forskere kan se som blå fluorescens i dette forstørrede tværsnit. Kredit:Tilpasset fra ACS Central Science 2020,
Fluorescerende teknik bringer ældningspolymerer frem i lysetOpvarmning af et tyndt stykke polypropylen i 30-150 minutter forårsager ældning, som forskere kan se som blå fluorescens i dette forstørrede tværsnit. Kredit:Tilpasset fra ACS Central Science 2020, -
 Forskere kan tilpasse hulrum i nyt porøst materialeBillede af det porøse materiale i tværsnit forstørret 29.000 gange. Den hvide streg er guldpladen, som materialet er bygget op på. Kredit:Martin Ratsch Forskere ved Göteborgs Universitet har fremst
Forskere kan tilpasse hulrum i nyt porøst materialeBillede af det porøse materiale i tværsnit forstørret 29.000 gange. Den hvide streg er guldpladen, som materialet er bygget op på. Kredit:Martin Ratsch Forskere ved Göteborgs Universitet har fremst -
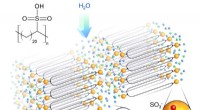 Ingeniører designer ny fast polymer elektrolyt, baner vejen for sikrere, mindre batterier og brænd…Forskernes nye struktur samles selv til hårnåleformer, resulterer i syreforede kanaler, der muliggør effektiv transport af protoner hen over elektrolytten. Kredit:Nature Materials Brændselsceller
Ingeniører designer ny fast polymer elektrolyt, baner vejen for sikrere, mindre batterier og brænd…Forskernes nye struktur samles selv til hårnåleformer, resulterer i syreforede kanaler, der muliggør effektiv transport af protoner hen over elektrolytten. Kredit:Nature Materials Brændselsceller -
 Hvor gammelt er det fingeraftryk?Kredit:CC0 Public Domain Retsmedicinske dramaer på tv gør det nemt at afgøre, hvornår fingeraftryk blev efterladt på gerningsstedet. I virkeligheden nedbrydes olierne i fingeraftryk over tid, og de
Hvor gammelt er det fingeraftryk?Kredit:CC0 Public Domain Retsmedicinske dramaer på tv gør det nemt at afgøre, hvornår fingeraftryk blev efterladt på gerningsstedet. I virkeligheden nedbrydes olierne i fingeraftryk over tid, og de
- Hvad gør Eris unik?
- Hvorfor testede Storbritanniens forsvarsminister psykiske kræfter?
- Hvilket kommer første jordskælv eller vulkaner?
- Udsving i tomrummet
- Hvor mange mol hydrogengas vil der blive produceret fra 250,0 milliliter en 3,0 M HCl i et overskud …
- Hvor mange mol vand er i denne reaktion 2C8H18 25O2- 16CO2 18H2O?


