Hvor mange mol hydrogengas vil der blive produceret fra 250,0 milliliter en 3,0 M HCl i et overskud af Mg?
$$2HCl + Mg \højrepil MgCl_2 + H_2$$
Ud fra ligningen kan vi se, at der kræves 2 mol HCl for at producere 1 mol brintgas. Derfor kan antallet af mol hydrogengas fremstillet af 250,0 milliliter 3,0 M HCl beregnes som følger:
$$Molaritet =\frac{Moler \ af \ Solute}{Liter \ af \ Solution}$$
$$Moler \ af \ HCl =Molaritet \ gange liter \ af \ Solution$$
$$Moler \ HCl =3,0 M \ gange 0,250 L =0,750 \ mol \ HCl$$
$$Moler \ af \ H_2 =\frac{0,750 \ mol \ HCl}{2} =0,375 \ mol \ H_2$$
Derfor vil der blive produceret 0,375 mol brintgas fra 250,0 milliliter 3,0 M HCl i et overskud af Mg.
Sidste artikelHvad det samlede antal valens e OF2?
Næste artikelHvor mange brintatomer er der i 7,00 mol ammoniumsulfid?
 Varme artikler
Varme artikler
-
 Forskere gennemgår de hurtige fremskridt inden for maskinlæring for de kemiske videnskaberKredit:CC0 Public Domain Et nyt værktøj ændrer ansigtet på kemisk forskning drastisk - kunstig intelligens. I et nyt blad udgivet i Natur , forskere gennemgår de hurtige fremskridt inden for mas
Forskere gennemgår de hurtige fremskridt inden for maskinlæring for de kemiske videnskaberKredit:CC0 Public Domain Et nyt værktøj ændrer ansigtet på kemisk forskning drastisk - kunstig intelligens. I et nyt blad udgivet i Natur , forskere gennemgår de hurtige fremskridt inden for mas -
 Analyse af fordele og ulemper ved to sammensatte fremstillingsmetoderKredit:Pixabay/CC0 Public Domain Flyvinger, vindmøllevinger, og andre store dele er typisk fremstillet ved hjælp af bulkpolymerisation i kompositproduktionsfaciliteter. De opvarmes og hærdes i eno
Analyse af fordele og ulemper ved to sammensatte fremstillingsmetoderKredit:Pixabay/CC0 Public Domain Flyvinger, vindmøllevinger, og andre store dele er typisk fremstillet ved hjælp af bulkpolymerisation i kompositproduktionsfaciliteter. De opvarmes og hærdes i eno -
 Maskinlæring giver en genvej til at simulere interaktioner i materialer til solenergihøstMaskinlæring kan omgå eksplicit beregning af visse materialers adfærd for at accelerere simuleringer af optiske egenskaber af komplekse materialer ved endelig temperatur. Kredit:Argonne National Labor
Maskinlæring giver en genvej til at simulere interaktioner i materialer til solenergihøstMaskinlæring kan omgå eksplicit beregning af visse materialers adfærd for at accelerere simuleringer af optiske egenskaber af komplekse materialer ved endelig temperatur. Kredit:Argonne National Labor -
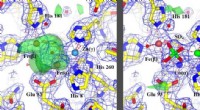 Ny røntgenmetode har dybtgående konsekvenser for udviklingen af livreddende lægemidlerDen nye metode, korrigere de forkert identificerede metaller, tilladt genfortolkning af uidentificerede funktioner, fremhævet med grønt, (billede til venstre) for at identificere, hvordan proteinet vi
Ny røntgenmetode har dybtgående konsekvenser for udviklingen af livreddende lægemidlerDen nye metode, korrigere de forkert identificerede metaller, tilladt genfortolkning af uidentificerede funktioner, fremhævet med grønt, (billede til venstre) for at identificere, hvordan proteinet vi
- Astral projektion:En tilsigtet uden for kroppen oplevelse
- Vand glider frit hen over nanodrapes lavet af verdens tyndeste materiale
- Udvikling af teknologi til fremstilling af interconnect i mikroskala fra flerlagsgrafen
- Djorgovski 2 er en moderat metalfattig kuglehob, undersøgelse finder
- Plantepigmenter fundet i spinat
- Hvordan man laver en regnskov til et videnskabsprojekt


