Hvor mange brintatomer er der i 7,00 mol ammoniumsulfid?
$$7,00 \text{ mol (NH}_4)_2\text{S} \times \frac{8 \text{ mol H}}{1 \text{ mol (NH}_4)_2\text{S}} =\ boxed{56 \text{ mol H}}$$
 Varme artikler
Varme artikler
-
 Svampeforbindelser hæmmer en vigtig gruppe af proteinerSvampen, der producerer cercosporamid. Kredit:Jelmer Hoeksma, copyright Hubrecht Institute Forskere i Jeroen den Hertogs gruppe, i samarbejde med forskere i Leiden, har fundet ud af, at en forbind
Svampeforbindelser hæmmer en vigtig gruppe af proteinerSvampen, der producerer cercosporamid. Kredit:Jelmer Hoeksma, copyright Hubrecht Institute Forskere i Jeroen den Hertogs gruppe, i samarbejde med forskere i Leiden, har fundet ud af, at en forbind -
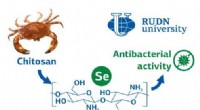 Kemikere syntetiserer en antimikrobiel forbindelse ud fra harmløst kitin og selenKredit:Russian Foundation for Basic Research RUDN-kemikere opnåede stoffer med høj antibakteriel aktivitet baseret på chitosan og selen. En af dem klarede sig endda bedre end almindelige antibiotik
Kemikere syntetiserer en antimikrobiel forbindelse ud fra harmløst kitin og selenKredit:Russian Foundation for Basic Research RUDN-kemikere opnåede stoffer med høj antibakteriel aktivitet baseret på chitosan og selen. En af dem klarede sig endda bedre end almindelige antibiotik -
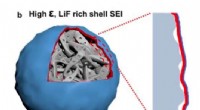 Et nyt elektrolytdesign, der kunne forbedre ydeevnen af Li-ion-batterierBillede, der viser en Si-partikel dækket af den LiF-rige SEI. Kredit:Chen et al. De fleste eksisterende lithium-ion-batterier (LIBer) integrerer grafitanoder, som har en kapacitet på cirka 350 mil
Et nyt elektrolytdesign, der kunne forbedre ydeevnen af Li-ion-batterierBillede, der viser en Si-partikel dækket af den LiF-rige SEI. Kredit:Chen et al. De fleste eksisterende lithium-ion-batterier (LIBer) integrerer grafitanoder, som har en kapacitet på cirka 350 mil -
 Stenåndende bakterier er elektronspindoktorer, viser undersøgelseElektroner, der bevæger sig gennem protein-ledninger mellem bakterieceller og overflader uden for disse celler, har en tendens til at have et bestemt kvantespin. Kredit:Katya Kadyshevskaya Elektro
Stenåndende bakterier er elektronspindoktorer, viser undersøgelseElektroner, der bevæger sig gennem protein-ledninger mellem bakterieceller og overflader uden for disse celler, har en tendens til at have et bestemt kvantespin. Kredit:Katya Kadyshevskaya Elektro
- Afrikas ældste dinosaur fundet i Zimbabwe
- University of Pennsylvania ingeniører afslører, hvad der gør diamanter glatte på nanoskala
- Hvad hedder processen, hvor deleceller danner haploide celler?
- Metan i fanerne på Saturns måne Enceladus:Mulige tegn på liv?
- At studere abstrakte matematiske ligninger ved hjælp af håndgribelige overflader
- Hvad er de særlige ting, der sker, når cellerne deles?


