Sådan konverteres atommasseenheder til joule:en praktisk vejledning
Af J.R. Kambak , opdateret 30. august 2022
Atommasseenheder (amu) giver en bekvem måde at udtrykke massen af subatomære partikler på. For at konvertere amu til SI-energienheden joule (J), stoler vi på Einsteins masseenergiækvivalens:E = mc². Denne korte guide guider dig gennem konverteringen trin for trin, inklusive et eksempel fra den virkelige verden med lithium-7.
Trin-for-trin konvertering af 1 amu til Joule
1. Genkend massefejlen
Massen af en kerne er altid mindre end summen af dens protoner og neutroner. Nøjagtige massemålinger er afgørende; afrunding tidligt kan eliminere den lille massefejl.
2. Konverter amu til kilogram
Brug den præcise konvertering:1amu = 1,66053886 × 10⁻²⁷kg.
3. Anvend Einsteins ligning
Indsæt massedefekten (her 1 amu) og lysets hastighed (c = 2,99792458 × 10⁸ms⁻¹) i E = mc²:
E = 1.66053886 × 10⁻²⁷ kg × (2.99792458 × 10⁸ m s⁻¹)²
4. Beregn energien
Udførelse af beregningen giver E = 1,492393 × 10⁻¹⁰kgm²s⁻².
5. Konverter til joule
Da 1kgm²s⁻² er lig med 1J, er det endelige resultat:
1amu = 1,492393 × 10⁻¹⁰J
Eksempel:Bindingsenergi af Lithium-7
1. Bestem massedefekten
• Nuklear masse af ⁷Li = 7,014353amu• Samlet masse af dens nukleoner:(3 × 1,007276) + (4 × 1,008665) = 7,056488amu• Masse defekt = 7,056488 – 7,014353 = 0,042135amu
2. Konverter til kilogram
0,042135amu × 1,66053886 × 10⁻²⁷kg= 6,99693 × 10⁻²⁸kg
3. Beregn energien
E = 6,99693 × 10⁻²⁸kg × (2,99792458 × 10⁸ms⁻¹)² = 6,28842 × 10⁻¹²J
Således er bindingsenergien for lithium-7 cirka 6,29 × 10⁻¹²J.
Disse beregninger illustrerer, hvordan massedefekten oversættes direkte til bindingsenergi, hvilket understreger den dybe sammenhæng mellem masse og energi, der beskrives af relativitetsteorien.
 Varme artikler
Varme artikler
-
 Forskere skaber fotoniske materialer til kraftfuld, effektiv lysbaseret databehandlingKredit:CC0 Public Domain Forskere fra University of Central Florida udvikler nye fotoniske materialer, der en dag kan hjælpe med at muliggøre laveffekt, ultrahurtig, lys-baseret databehandling. De
Forskere skaber fotoniske materialer til kraftfuld, effektiv lysbaseret databehandlingKredit:CC0 Public Domain Forskere fra University of Central Florida udvikler nye fotoniske materialer, der en dag kan hjælpe med at muliggøre laveffekt, ultrahurtig, lys-baseret databehandling. De -
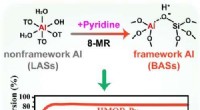 Dynamisk udvikling af aluminiumskoordinationsmiljøer i mordenitzeolitGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210658 Zeolitter er vigtige i mange kemiske syntese og petrokemiske processer. De økonomiske og miljømæs
Dynamisk udvikling af aluminiumskoordinationsmiljøer i mordenitzeolitGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202210658 Zeolitter er vigtige i mange kemiske syntese og petrokemiske processer. De økonomiske og miljømæs -
 Ny 3D-trykningsteknik producerer levende 4-D materialerUNSW-forskere har kombineret 3D-print med en lysstyret proces for at skabe en levende 4D-harpiks. Kredit:Shutterstock Reparation og genbrug af plast og levering af kræftmedicin mere effektivt er k
Ny 3D-trykningsteknik producerer levende 4-D materialerUNSW-forskere har kombineret 3D-print med en lysstyret proces for at skabe en levende 4D-harpiks. Kredit:Shutterstock Reparation og genbrug af plast og levering af kræftmedicin mere effektivt er k -
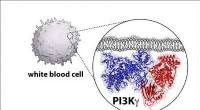 Kemikere udvikler en ny plan for enzym involveret i kræftKredit:University of Oregon Forskere har i årtier vidst, at en bestemt klasse af enzymer er en vigtig aktør inden for cellebiologi, fordi de ofte muterer og bliver væsentlige årsager til kræft. B
Kemikere udvikler en ny plan for enzym involveret i kræftKredit:University of Oregon Forskere har i årtier vidst, at en bestemt klasse af enzymer er en vigtig aktør inden for cellebiologi, fordi de ofte muterer og bliver væsentlige årsager til kræft. B
- Fiskeri efter en dårlig celle ud af billioner af gode
- Hvad er et andet navn på bakteriekongeriget?
- Hvad er sammensat med overførsel af elektron et metalelement og ikke -element?
- Undersøgelse identificerer religiøse skævheder mod flygtninge
- FORKLARER:Den virkelige matematik bag netto nul CO2-emissioner
- Hvis tyngdekraften øges, hvilken måling der vil ændre sig, og hvordan?


