Hvordan pH-ændringer påvirker biologiske systemer
Af Jacob Stutsman, Opdateret 30. august 2022
pH-skalaen kvantificerer en opløsnings surhedsgrad ved at måle dens hydrogenionkoncentration. Biologiske systemer afhænger af et snævert pH-område; selv beskedne afvigelser kan forstyrre cellulære processer, enzymaktivitet og organfunktion.
Forstå pH
I vandig kemi hæver syrer koncentrationen af hydrogenioner (H⁺), mens baser øger hydroxidioner (OH⁻). Skalaen går fra 0 til 14, hvor 7 betragtes som neutral ved 77°F. Hver enhedsændring repræsenterer en tidobbel forskel i ionaktivitet.
Sure-base-homeostase
Organismer opretholder pH-homeostase gennem buffersystemer og respiratoriske eller renale justeringer. Bicarbonatbufferen reagerer f.eks. med CO2 til dannelse af kulsyre, som dissocierer i H+ og HCO3⁻. Enzymatisk katalyse kan vende reaktionen, så kroppen kan finjustere surhed eller alkalinitet. Disse mekanismer holder systemisk pH inden for stramme grænser.
Blod pH og sundhed
Menneskeblod er stramt reguleret mellem 7.35 og 7.45. Afvigelser – acidose (pH<7,35) eller alkalose (pH>7,45) – påvirker proteinladning, adskillelse af røde blodlegemer og funktionen af organer såsom hjerte og nyrer. Kroniske skift kan også ændre knoglemineralisering, hvilket påvirker knogletætheden.
Mavesyrefunktion
Mavens saltsyre (pH1-2) starter proteindenaturering og enzymatisk fordøjelse. Antacida neutraliserer overskydende syre og giver lindring for gastro-øsofageal refluks eller mavesår.
Påvirkning af vandliv
Surt vand (pH<4,5) forstyrrer osmotisk balance i fisk og andre vandlevende organismer, og tvinger celler til at absorbere H⁺ på bekostning af Na⁺, hvilket fører til respirationssvigt og dødelighed. Let alkaliske forhold kan også forringe iontransport og metaboliske processer.
At forstå, hvordan pH-skift påvirker biologiske systemer, er afgørende for medicinske, miljømæssige og industrielle anvendelser.
 Varme artikler
Varme artikler
-
 Hvorfor overgangsmetaller er fremragende katalysatorerJason Reed/Photodisc/Getty Images Overgangsmetaller - elementer som krom, jern og nikkel - har valenselektroner i to skaller, hvilket giver dem unikke katalytiske egenskaber. Fordi de let kan donere
Hvorfor overgangsmetaller er fremragende katalysatorerJason Reed/Photodisc/Getty Images Overgangsmetaller - elementer som krom, jern og nikkel - har valenselektroner i to skaller, hvilket giver dem unikke katalytiske egenskaber. Fordi de let kan donere -
 Cyanobakterier kan revolutionere plastindustrienSimpel laboratoriedyrkning af cyanobakterier i luftede rør. Kredit:Universitetet i Tübingen Cyanobakterier producerer plast naturligt som et biprodukt af fotosyntesen - og de gør det på en bæredyg
Cyanobakterier kan revolutionere plastindustrienSimpel laboratoriedyrkning af cyanobakterier i luftede rør. Kredit:Universitetet i Tübingen Cyanobakterier producerer plast naturligt som et biprodukt af fotosyntesen - og de gør det på en bæredyg -
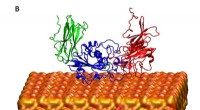 XSEDE-supercomputertildelinger på Stampede1 og Comet hjælper med at prøve proteinfoldning i knogl…XSEDE-supercomputere Stampede ved TACC og Comet ved SDSC hjalp studieforfattere med at simulere hovedstykkedomænet af cellemembranproteinreceptorintegrinet i opløsning, baseret på molekylær dynamik mo
XSEDE-supercomputertildelinger på Stampede1 og Comet hjælper med at prøve proteinfoldning i knogl…XSEDE-supercomputere Stampede ved TACC og Comet ved SDSC hjalp studieforfattere med at simulere hovedstykkedomænet af cellemembranproteinreceptorintegrinet i opløsning, baseret på molekylær dynamik mo -
 Nyopdaget enzym bruger en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugtKredit:CC0 Public Domain Nyopdaget enzym anvender en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugt i øjnene Det ildelugtende molekyle, der giver husdyrgødning sin frast
Nyopdaget enzym bruger en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugtKredit:CC0 Public Domain Nyopdaget enzym anvender en usædvanlig mekanisme til at generere et molekyle med en forfærdelig lugt i øjnene Det ildelugtende molekyle, der giver husdyrgødning sin frast
- Hvordan ved du, at den tredje lov om termodynamik er sandt?
- Hvad hedder Moon Landing?
- CES tech show:Sig nej til junkfood; maskiner laver cocktails
- Hvilken del af cellen er stærk og stiv svær at komme igennem kun fundet i planter?
- Forholdet mellem elektricitet og magnetisme
- Forlader du solcelledækning om dagen for at absorbere varme eller bare om natten, så undslippe?


