Beregning af varmeafgivelse i zink-saltsyrereaktionen
Af Oxana Fox, opdateret 30. august 2022
Saltsyre (HCl) reagerer let med zink (Zn) for at producere zinkchlorid (ZnCl2) og hydrogengas (H2). Denne reaktion er eksoterm; den frigivne varme kvantificeres af reaktionsentalpien.
Trin 1 – Skriv den balancerede ligning
Zn + 2 HCl → ZnCl₂ + H₂
Trin 2 – Indsaml standardentalpier for dannelse
Standardentalpier (ΔH°ₓf) er angivet i kilojoule pr. mol (kJmol⁻1). For denne reaktion er de:
- Zn (0 kJmol⁻¹)
- HCl (−167,2 kJmol⁻¹)
- ZnCl₂ (−415,1 kJmol⁻¹)
- H₂ (0 kJmol⁻¹)
Trin 3 – Beregn den samlede entalpi af reaktanterne
ΣΔH°ₓf (reaktanter) = 0 + 2(−167,2) = −334,3 kJmol⁻¹
Trin 4 – Beregn den samlede entalpi for produkterne
ΣΔH°ₓf (produkter) = −415,1 + 0 = −415,1 kJmol⁻¹
Trin 5 – Bestem reaktionsentalpien
ΔH°rxn = ΣΔH°ₓf (produkter) − ΣΔH°ₓf (reaktanter) = −415,1 − (−334,3) = −80,8 kJmol⁻¹
Det negative fortegn indikerer, at reaktionen frigiver cirka 81 kJ varme pr. mol forbrugt zink.
For mere detaljerede termodynamiske data, se NIST Chemistry WebBook .
 Varme artikler
Varme artikler
-
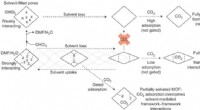 Kontinuerlig åndbar metal-organisk ramme med gæsteselektivitetForeslået rolle for gæst-ramme-interaktioner i de opløsningsmiddelafhængige kontinuerlige vejrtrækningsegenskaber af SHF-61. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2747 (Phys.org) —Forsk
Kontinuerlig åndbar metal-organisk ramme med gæsteselektivitetForeslået rolle for gæst-ramme-interaktioner i de opløsningsmiddelafhængige kontinuerlige vejrtrækningsegenskaber af SHF-61. Kredit:(c) Naturkemi (2017). DOI:10.1038/nchem.2747 (Phys.org) —Forsk -
 Inspireret af naturlige signaler i levende celler, forskere designer kunstig gasdetektorKemikere fra University of Tokyo har designet bittesmå nanokuber, der naturligt lyser blåt under UV-lys. Gløden er 3,9 gange stærkere, når kuberne er fyldt med brændbar gas. Nanokuberne er et første s
Inspireret af naturlige signaler i levende celler, forskere designer kunstig gasdetektorKemikere fra University of Tokyo har designet bittesmå nanokuber, der naturligt lyser blåt under UV-lys. Gløden er 3,9 gange stærkere, når kuberne er fyldt med brændbar gas. Nanokuberne er et første s -
 Flydende retsmedicin kan føre til mere sikkert drikkevandInstrumentet er designet til at analysere kvaliteten af væsker ved hjælp af den fotoakustiske effekt, eller dannelse af lydbølger efter lys er absorberet i et materiale. MU -forskerne mener, at dett
Flydende retsmedicin kan føre til mere sikkert drikkevandInstrumentet er designet til at analysere kvaliteten af væsker ved hjælp af den fotoakustiske effekt, eller dannelse af lydbølger efter lys er absorberet i et materiale. MU -forskerne mener, at dett -
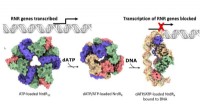 Ny mekanisme til regulering af forsyningen af DNA-byggesten til bedre antibiotikaVirkningsmekanismen af den RNR-specifikke repressor NrdR. Overfladerepræsentation af cryo-EM-kortene for de dodecameriske, oktamere og DNA-bundne tetramere NrdR-strukturer. NrdR-monomerer i hver tet
Ny mekanisme til regulering af forsyningen af DNA-byggesten til bedre antibiotikaVirkningsmekanismen af den RNR-specifikke repressor NrdR. Overfladerepræsentation af cryo-EM-kortene for de dodecameriske, oktamere og DNA-bundne tetramere NrdR-strukturer. NrdR-monomerer i hver tet
- Hvad er den molekylære formel, hvis vandig hypochlorosyre og vandig calciumhydroxidreaktion?
- Hvilken masse ilt kræves for at forbrænde 28,8 g ammoniak?
- En prøve på 50,0 ml på 0,436 M NH4NO3 fortyndes med vand til en samlet volumen 250,0 Hvad ammoniu…
- Hvad er det rigtige navn på sammensat cacl2x6h2o?
- Hvordan påvirker tidevand aktiviteter?
- Hvad er en stjerne, som gravitationsmæssigt bundet til en anden, enten kan være en del af en klyng…


