Sublimation in Science:Hvordan faste stoffer springer væskefasen over
Af Allison Boley | Opdateret 30. august 2022
Hvad er sublimering?
Sublimering er den direkte overgang af et stof fra den faste fase til den gasfase, der helt omgår den flydende tilstand. Processen opstår, når temperaturen og trykket af et materiale placerer det i et område af fasediagrammet, hvor de faste og gasfaser er i ligevægt.
Særlige forhold
Alt velkendt stof eksisterer i en af tre hovedfaser:fast, flydende eller gas. Disse faser er forskellige tilstande af det samme kemiske stof. For eksempel eksisterer vand som is (fast ), flydende vand eller damp (gas ), alle med den samme kemiske formel, H2 O.
Faseovergange
De mest almindelige overgange er smeltning (fast til flydende) og kogning (væske til gas). Sublimering derimod bevæger sig direkte fra fast stof til gas. Den omvendte proces – gas til fast stof – kaldes aflejring.
Fasediagrammer forklaret
Et fasediagram kortlægger temperatur (x-akse) mod tryk (y-akse) for at illustrere, hvor hver fase findes. For at fremkalde sublimering skal systemet være under fast-væske-grænsen og under væske-gas-grænsen, typisk ved lavt tryk. Den enkelte fastgas-linje på diagrammet markerer betingelserne for direkte konvertering.
Latent sublimationsvarme
Når varme tilsættes til et fast stof, stiger dets temperatur, indtil det når overgangslinjen fast-gas. På det tidspunkt øger yderligere energitilførsel ikke temperaturen, men tilfører i stedet den latente varme, der kræves for at bryde bindingerne, der holder faststoffet sammen. Denne energi er den latente sublimationsvarme. Når gassen kondenserer tilbage til fast form, frigives den samme mængde varme.
Eksempler fra den virkelige verden
- Tøris: Fast kuldioxid (CO2 ), der sublimerer ved -78,5°C og producerer en kold, usynlig gas uden væskefase.
- Jod: Et violet fast stof, der kan sublimere ved stuetemperatur, ofte set som en svag lilla damp.
- Naftalen: Brugt i mølkugler sublimerer denne organiske forbindelse let og frigiver en karakteristisk lugt.
- Frysetørring: Fødevarer fryses og udsættes derefter for et vakuum, så isen sublimeres direkte til vanddamp, hvilket bevarer tekstur og smag.
Disse eksempler illustrerer, hvordan sublimering ikke kun er et grundlæggende fysisk fænomen, men også et praktisk værktøj i videnskab og industri.
 Varme artikler
Varme artikler
-
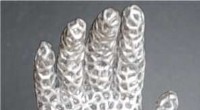 Forskning i flydende metal påberåber Terminator -film - men meget venligereEn hånd, der langsomt åbner sig, når metalgitteret smelter. Kredit:Pu Zhang Pu Zhang kan lide at sammenligne sit teams forskning om flydende metaller med Terminator - specifikt 1991s Terminator 2:
Forskning i flydende metal påberåber Terminator -film - men meget venligereEn hånd, der langsomt åbner sig, når metalgitteret smelter. Kredit:Pu Zhang Pu Zhang kan lide at sammenligne sit teams forskning om flydende metaller med Terminator - specifikt 1991s Terminator 2: -
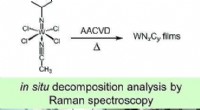 Simuleret kemisk dampaflejring fra en wolframcarbonitridforløberKredit: European Journal of Inorganic Chemistry Tynde film spiller en central rolle i produktionen af elektronik. De kan dyrkes direkte på en substratoverflade gennem processen med kemisk dampa
Simuleret kemisk dampaflejring fra en wolframcarbonitridforløberKredit: European Journal of Inorganic Chemistry Tynde film spiller en central rolle i produktionen af elektronik. De kan dyrkes direkte på en substratoverflade gennem processen med kemisk dampa -
 Kugler kan gøre beton slankere, grønnerePakket, mikronskala calciumsilikatkugler udviklet ved Rice University er et lovende materiale, der kan føre til stærkere og mere miljøvenlig beton. Kredit:Multiscale Materials Laboratory/Rice Universi
Kugler kan gøre beton slankere, grønnerePakket, mikronskala calciumsilikatkugler udviklet ved Rice University er et lovende materiale, der kan føre til stærkere og mere miljøvenlig beton. Kredit:Multiscale Materials Laboratory/Rice Universi -
 De fire elementer, der udgør bagepulverAf Kylene Arnold Opdateret 24. marts 2022 Geografisk/iStock/GettyImages Bagepulver, videnskabeligt kendt som natriumbicarbonat, er en alsidig basisvare i husholdningen. I modsætning til bagepulver
De fire elementer, der udgør bagepulverAf Kylene Arnold Opdateret 24. marts 2022 Geografisk/iStock/GettyImages Bagepulver, videnskabeligt kendt som natriumbicarbonat, er en alsidig basisvare i husholdningen. I modsætning til bagepulver
- Er en polymermaling den samme som gouache?
- Polymer, der heler som hud meget tæt på produktion i industriel skala
- Hvilket delsystem inkluderer alle levende ting på jorden?
- Fem anvendelsesområder for lineære programmeringsteknikker
- Hvad er der i organismer lavet af?
- Ny metode genererer effektivt hydrogen fra vand


