Sådan beregnes bikarbonatkoncentration ud fra CO₂-partialtryk
Af John Brennan, opdateret 30. august 2022
I et kemisk system opnås ligevægt, når de fremadrettede og omvendte reaktioner forløber med samme hastighed. Placeringen af denne ligevægt er styret af termodynamik - specifikt den frigivne energi og entropien ændres under processen. Ved en given temperatur og tryk er forholdet mellem reaktanter og produkter fastsat af ligevægtskonstanten. Når partialtrykket af CO₂ er kendt, kan ligevægtskonstanten bruges til at beregne koncentrationen af bicarbonat, HCO₃⁻, i opløsning.
Trin 1:Skriv de relevante ligevægte
- CO₂ (g) + H₂O (l) ⇌ H₂CO₃ (vandig)
- H₂CO₃ (aq) ⇌ H⁺ (aq) + HCO₃⁻ (aq)
- HCO₃⁻ (aq) ⇌ H⁺ (aq) + CO₃²⁻ (aq)
Alle disse reaktioner er reversible. Ligevægtskonstanterne for hvert trin giver os mulighed for at bestemme de relative koncentrationer af CO₂, H₂CO₃, HCO₃⁻ og CO₃²⁻ ved ligevægt.
Trin 2:Lav praktiske antagelser
Under antagelse af stuetemperatur (≈25°C) og standardatmosfærisk tryk, betragter vi typisk kun carbonat (CO₃²⁻) for at være til stede i spormængder, når opløsningens pH er ≤9. Under disse betingelser dominerer opløst CO2, kulsyre (H2CO3) og bicarbonat (HCO3-). I stærkt alkaliske medier (pH>9) skifter balancen mod bicarbonat og carbonat, hvor kulsyre bliver ubetydelig.
Trin 3:Beregn koncentrationen af opløst CO₂
Ved at bruge Henrys lov er koncentrationen af opløst CO₂ givet ved:
CO₂(aq) =(2,3×10⁻²molL⁻¹atm⁻¹)×P_CO₂
hvor P_CO₂ er partialtrykket af CO₂ i atmosfærer.
Trin 4:Estimer kulsyrekoncentrationen
Kulsyre dannes ud fra opløst CO₂ i henhold til ligevægtskonstanten for den første reaktion. Et empirisk forhold er:
H2CO3 =(1,7x10-3molL-1mol-1L)×[CO2(vandig)]
Trin 5:Bestem bikarbonatkoncentrationen
Fordi H2CO3 er en svag syre, kan dens dissociation i H⁺ og HCO3⁻ tilnærmes ved hjælp af syredissociationskonstanten (K_a ≈ 4,3×10⁻⁷). Omarrangering af udtrykket for K_a giver:
4,3×10⁻⁷ =[H⁺]² / [H₂CO₃]
Forudsat elektroneutralitet, [H⁺] ≈ [HCO₃⁻] ved dette pH-område. Løsning for [HCO₃⁻] giver den ønskede bicarbonatkoncentration:
[HCO₃⁻] =√(4,3×10⁻⁷×[H₂CO₃])
TL;DR
Ved ligevægt balancerer systemet de fremadrettede og omvendte reaktioner, og forbinder CO₂-partialtryk, opløst CO₂, kulsyre og bicarbonat. Ved at anvende Henrys lov og syredissociationskonstanten kan du beregne bicarbonatkoncentrationen i en opløsning.
 Varme artikler
Varme artikler
-
 Forskere opdager en ny fase i blokcopolymererKunstnerens koncept, der skildrer blokpolymerer pakket sammen til dannelse, I dette tilfælde, en ny fase af diblok-copolymer. Kredit:Brian Long Alt stof består af en eller flere faser - områder af
Forskere opdager en ny fase i blokcopolymererKunstnerens koncept, der skildrer blokpolymerer pakket sammen til dannelse, I dette tilfælde, en ny fase af diblok-copolymer. Kredit:Brian Long Alt stof består af en eller flere faser - områder af -
 Kemiker foreslår en ny metode til grøn syntese af xanthenderivaterKredit:RUDN University En RUDN -kemiker har foreslået en ny metode til syntese af xanthenderivater, som bruges som grundlag for fremstilling af lægemidler - fra antidepressiva til antivirale og an
Kemiker foreslår en ny metode til grøn syntese af xanthenderivaterKredit:RUDN University En RUDN -kemiker har foreslået en ny metode til syntese af xanthenderivater, som bruges som grundlag for fremstilling af lægemidler - fra antidepressiva til antivirale og an -
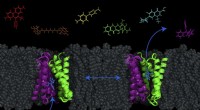 Ny model afslører muligheden for at pumpe antibiotika ind i bakterierEt transportørprotein - kaldet EmrE, vist i lilla og grønt -- i cellemembranen af E. coli kan bakterier skiftes mellem to konformationer for at pumpe molekyler (såsom antibakterielle lægemidler) ud
Ny model afslører muligheden for at pumpe antibiotika ind i bakterierEt transportørprotein - kaldet EmrE, vist i lilla og grønt -- i cellemembranen af E. coli kan bakterier skiftes mellem to konformationer for at pumpe molekyler (såsom antibakterielle lægemidler) ud -
 Integreret brintlager til brændselscellebilerKredit:CC0 Public Domain Der er en drivkraft for at fortrænge fossile brændstoffer i elproduktion og transport med bæredygtige alternativer. En tilgang, der er blevet diskuteret i løbet af de sids
Integreret brintlager til brændselscellebilerKredit:CC0 Public Domain Der er en drivkraft for at fortrænge fossile brændstoffer i elproduktion og transport med bæredygtige alternativer. En tilgang, der er blevet diskuteret i løbet af de sids
- Hvad er forskellen fra en dipioD og HaplioD -celle?
- Ny matematisk model:Hvordan farlige bakterier danner kolonier
- Hvilke almindelige genstande findes svovl i?
- Ny open source-software forudsiger virkningerne af ekstreme begivenheder på net
- Hvordan laver man en 3,5 millimolær opløsning af 1 molær svovlsyre?
- Hvad er det ekstra i min online kurv? Snart, måske en moms


