Hvordan elektroner er fordelt i et atoms skaller
Af Michael E Carpenter, Opdateret 30. august 2022
Elektroner er negativt ladede subatomære partikler, der optager diskrete energiniveauer - ofte visualiseret som skaller - der omgiver atomkernen. En skal skal fyldes, før en elektron kan bevæge sig til et højere energiniveau. Kapaciteten af hver skal er forskellig, og de faktiske elektronfordelinger afviger fra simple cirkulære baner.
Elektroner pr. skal
Den første skal kan rumme op til to elektroner; hydrogen (1e⁻) og helium (2e⁻) har kun denne skal. Den anden skal rummer otte elektroner, den tredje 18 og den fjerde 32.
Underskaller
Inden for hver skal repræsenterer underskaller - betegnet s, p, d og f - finere energiinddelinger. s-underskallen rummer to elektroner; p rummer seks; d rummer ti; f rummer fjorten. Hver efterfølgende underskal kan indeholde fire flere elektroner end den foregående.
Sub-Shell-notation
Et atoms elektronkonfiguration er skrevet som en sekvens af skalnummer, underskalbogstav og elektronantal. For eksempel er bor (5e⁻) beskrevet som 1s² 2s² 2p¹ , hvilket indikerer to elektroner i den første skals underskal, to i den anden skals underskal og en i den anden skals p-underskal.
Sub-Shell Shape
Formerne for sandsynlighedstæthed er forskellige mellem underskaller. s underskaller er sfæriske; p sub-shells ligner håndvægte. Hver p-orbital kan være vært for to elektroner, så en fuld p-underskal indeholder tre sådanne orbitaler, i alt seks elektroner.
Electron Cloud
Elektroner følger ikke faste cirkulære baner; i stedet eksisterer de som en sandsynlighedssky. På et s underniveau optager de to elektroner et sfærisk område, men de kan findes hvor som helst inden for det volumen på ethvert tidspunkt. Kvantemekanikken tillader elektronen at eksistere ud over den klassiske grænse, hvilket skaber en diffus sky af sandsynlighed, der gælder for alle underskaller.
 Varme artikler
Varme artikler
-
 Forskere gennemfører fase 1 menneskelige forsøg med smarte pillerFase et menneskelige forsøg med smarte piller, der kunne revolutionere forebyggelsen og diagnosen tarmsygdomme og sygdomme, er blevet gennemført af forskere i Melbourne, Australien Kredit:RMIT Univers
Forskere gennemfører fase 1 menneskelige forsøg med smarte pillerFase et menneskelige forsøg med smarte piller, der kunne revolutionere forebyggelsen og diagnosen tarmsygdomme og sygdomme, er blevet gennemført af forskere i Melbourne, Australien Kredit:RMIT Univers -
 Cement kontra beton:Deres forskelle, og muligheder for bæredygtighedEfter vand, beton er det mest forbrugte materiale på jorden. Forskere i MIT Concrete Sustainability Hub undersøger, hvordan man kan reducere dens indvirkning. Kredit:Pix/Pexels liv Der er meget, d
Cement kontra beton:Deres forskelle, og muligheder for bæredygtighedEfter vand, beton er det mest forbrugte materiale på jorden. Forskere i MIT Concrete Sustainability Hub undersøger, hvordan man kan reducere dens indvirkning. Kredit:Pix/Pexels liv Der er meget, d -
 Mod forbedret sårheling:Kemisk syntese af et trefoil faktor peptidUndersøgelser viste, at trefoil-faktor-peptider produceres lokalt for at bekæmpe inflammation og skader i mave-tarmkanalen ved at fremskynde sårheling. Kredit:Universität Wien Den fascinerende fam
Mod forbedret sårheling:Kemisk syntese af et trefoil faktor peptidUndersøgelser viste, at trefoil-faktor-peptider produceres lokalt for at bekæmpe inflammation og skader i mave-tarmkanalen ved at fremskynde sårheling. Kredit:Universität Wien Den fascinerende fam -
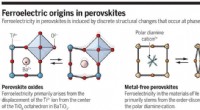 En måde at lave renere metalfrie perovskitter til en lav prisFerroelektricitet i perovskitter induceres af diskrete strukturelle ændringer, der sker ved faseovergange. Kredit:(c) C. Bickel/ Videnskab (2018). DOI:10.1126/science.aas9330 Et team af forskere
En måde at lave renere metalfrie perovskitter til en lav prisFerroelektricitet i perovskitter induceres af diskrete strukturelle ændringer, der sker ved faseovergange. Kredit:(c) C. Bickel/ Videnskab (2018). DOI:10.1126/science.aas9330 Et team af forskere


