Hvorfor is smelter hurtigere i vand end i sodavand:Videnskaben bag natrium- og hydrogenbindinger
Af Liz Veloz | Opdateret 30. august 2022
Oversigt
Is smelter mærkbart hurtigere, når den placeres i almindeligt vand sammenlignet med sodavand. Den vigtigste forskel ligger i tilstedeværelsen af natrium (salt) i sodavand, som sænker frysepunktet og kræver mere energi for at bryde vandets brintbindinger.
Hydrogenbindinger forklaret
Vandmolekyler er forbundet af svage brintbindinger, der konstant brydes og omdannes. Disse bindinger giver vandet dets enestående flydeevne og tillader det at forblive flydende fra 32°F til 212°F. Atomernes bevægelse bliver langsommere, efterhånden som temperaturen falder, hvilket i sidste ende fører til, at isen størkner.
Natriums indvirkning på smeltepunktet
Natriumioner i sodavand forstyrrer hydrogenbinding, hvilket reducerer antallet af frie vandmolekyler, der kan danne et fast gitter. Som et resultat falder smeltepunktet for is i sodavand til under 32°F, hvilket betyder, at is er længere tid om at smelte end i almindeligt vand.
Praktiske konsekvenser
I kolde områder spredes salt sædvanligvis på veje for at forhindre is i at dannes og holde overfladevæsken ved temperaturer, der ellers ville fryse. Det samme princip forklarer, hvorfor is smelter langsommere i sodavand:saltet holder opløsningen under den sædvanlige frysetærskel.
Vigtige ting
- Is smelter hurtigere i vand end i sodavand, fordi sodavandets natrium sænker smeltepunktet.
- At bryde brintbindinger kræver energi; tilsat salt øger dette energibehov.
- Saltets effekt bruges i applikationer fra den virkelige verden som f.eks. vejafisning.
Sidste artikelSådan afgøres, om et stof er surt:En praktisk vejledning
Næste artikelHvor kemisk fordøjelse sker:Fra mund til tolvfingertarm
 Varme artikler
Varme artikler
-
 Vand erstatter giftstoffer:Grøn produktion af plastStålreaktor i Miriam Unterlass laboratorium. Kredit:Vienna University of Technology Mange almindelige materialer er ikke bæredygtige. Nogle er skadelige for planter eller dyr, andre indeholder sjæ
Vand erstatter giftstoffer:Grøn produktion af plastStålreaktor i Miriam Unterlass laboratorium. Kredit:Vienna University of Technology Mange almindelige materialer er ikke bæredygtige. Nogle er skadelige for planter eller dyr, andre indeholder sjæ -
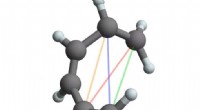 SLACs højhastighedselektronkamera filmer molekylær film i HDForskere skabte den første film med atomopløsning af ringåbningsreaktionen af 1, 3-cyclohexadien (CHD) med et elektronkamera kaldet UED. Nederst:UED-elektronstrålen måler nøjagtigt afstandene mellem
SLACs højhastighedselektronkamera filmer molekylær film i HDForskere skabte den første film med atomopløsning af ringåbningsreaktionen af 1, 3-cyclohexadien (CHD) med et elektronkamera kaldet UED. Nederst:UED-elektronstrålen måler nøjagtigt afstandene mellem -
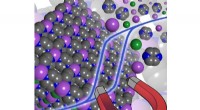 Mod næste generation af molekyle-baserede magneterBilledgengivelse af den molekylebaserede magnet og dens magnetiske egenskaber. Kredit:Rodolphe Clérac Magneter anvendes i en række teknologiske applikationer, inklusive satellitter, telefoner og k
Mod næste generation af molekyle-baserede magneterBilledgengivelse af den molekylebaserede magnet og dens magnetiske egenskaber. Kredit:Rodolphe Clérac Magneter anvendes i en række teknologiske applikationer, inklusive satellitter, telefoner og k -
 En stabil kobberkatalysator til omdannelse af kuldioxidKredit:CC0 Public Domain En ny katalysator til omdannelse af kuldioxid (CO 2 ) til kemikalier eller brændstoffer er blevet udviklet af forskere ved Ruhr-Universität Bochum og University of Duisb
En stabil kobberkatalysator til omdannelse af kuldioxidKredit:CC0 Public Domain En ny katalysator til omdannelse af kuldioxid (CO 2 ) til kemikalier eller brændstoffer er blevet udviklet af forskere ved Ruhr-Universität Bochum og University of Duisb
- Hvordan kan celle opbevare det sukker, der produceres i fotosyntesen?
- Hvilken energi frigiver mindre kerner for at danne en større kerne?
- Hvad kaldes grupper?
- Hvilket vejr er relateret til Nimbus -skyer?
- Den hastighed, hvormed hastigheden ændrer et givet øjeblik beskrevet af?
- Højtydende og wafer-skalerbare justerede carbon nanorør-transistorer


