Sådan afgøres, om et stof er surt:En praktisk vejledning
Af Philip J. Carlson, Opdateret 30. august 2022
Surhed er en strengt defineret kemisk egenskab, ikke et mål for, hvor ødelæggende et stof fremstår. Mens almindelige billeder forbinder syrer med korrosion og baser med rust, vurderer kemikere surhedsgraden ud fra hydrogenioners opførsel i opløsning.
Definition af syrer og baser
- Arrhenius :Syrer øger koncentrationen af ~+ ioner (protoner), når de opløses i vand; baser øger ∻- (hydroxid) ioner.
- Brønsted–Lowry :En syre donerer en proton til en anden art; en base accepterer en proton.
- Lewis :En syre er en elektronparacceptor; en base er en elektronpardonor.
Til de fleste hverdagsapplikationer er Arrhenius- og Brønsted-Lowry-definitionerne tilstrækkelige.
Praktisk test:Bagepulverreaktion
En af de enkleste måder at kontrollere, om en væske er sur, er at tilføje en lille mængde bagepulver (natriumbicarbonat). Hvis opløsningen indeholder en syre, vil den reagere og danne synlige bobler af kuldioxid:
Syre + NaHCO3 → Na + + CO2 + H2 O + OH -
Ingen bobler indikerer fravær af betydelig surhed.
Syrestyrker:Fra stærk til svag
En stærk syre dissocierer fuldstændigt i vand og frigiver alle dets protoner. En svag syre dissocierer kun delvist og efterlader en blanding af intakte molekyler og ioner. Stoffer, der indeholder brint, men som ikke udviser dissociation i vand, betragtes som ikke-sure.
PH-skalaen
pH-skalaen udtrykker kvantitativt surhedsgrad:
- pH <7:Surt
- pH =7:Neutral
- pH> 7:Grundlæggende (alkalisk)
Måler pH
Der findes flere pålidelige metoder:
- Lakmuspapir – Farveændring angiver omtrentlig pH, når den matches med et standarddiagram.
- Løsningsindikatorer – Tilføjelse af et farveændrende reagens direkte til væsken viser dens pH-klasse.
- Titrering – En præcis laboratorieteknik, der bestemmer pH ved at neutralisere prøven med en base eller syre af kendt koncentration.
- pH-måler – Den mest nøjagtige og brugervenlige metode; en elektrode måler det elektriske potentiale relateret til hydrogenionkoncentrationen.
Fælles pH-værdier
- Husholdningsblegemiddel:12,5 (stærkt grundlæggende)
- Mælk af magnesia:10 (basis)
- Natron:8 (grundlæggende)
- Rent vand:7 (neutral)
- Sort kaffe:5 (mildt surt)
- Vin:3,5 (sur)
- Cola, eddike:2,9 (sur)
- Mavesaft:1,2 (stærkt sur)
Referencer
- Brown, Theodore L.; LeMay, H. E. Jr.; Bursten, Bruce E. (2000). Kemi:Den centrale videnskab , 8. udg.
- Hyperfysik:pH
 Varme artikler
Varme artikler
-
 Nikkelatom hjælper med at reducere kuldioxidFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t
Nikkelatom hjælper med at reducere kuldioxidFigur 1:At vide, hvordan en nikkeljernsulfidkatalysator hjælper med at reducere kuldioxid til kulilte og andre kulbaserede produkter, kan føre til teknologier, der kan omdanne kuldioxid i atmosfæren t -
 Sammensætning styrer biologisk ur med lysFigur:Burforbindelser regulerer det cirkadiske ur med lys (billede af Issei Takahashi, Nagoya Universitet) Forskere ved Japans Institute of Transformative Bio-Molecules (ITbM) ved Nagoya Universit
Sammensætning styrer biologisk ur med lysFigur:Burforbindelser regulerer det cirkadiske ur med lys (billede af Issei Takahashi, Nagoya Universitet) Forskere ved Japans Institute of Transformative Bio-Molecules (ITbM) ved Nagoya Universit -
 Dybt dyk ned i vigtige COVID-19-proteiner er et skridt mod nye lægemidler, vaccinerNukleocapsid-phosphoproteinet (blåt) af SARS-CoV-2 (N) (grå) spiller kritiske roller i flere processer i SARS-CoV-2-infektionscyklussen, inklusive replikation og transskription, og pakning og beskytte
Dybt dyk ned i vigtige COVID-19-proteiner er et skridt mod nye lægemidler, vaccinerNukleocapsid-phosphoproteinet (blåt) af SARS-CoV-2 (N) (grå) spiller kritiske roller i flere processer i SARS-CoV-2-infektionscyklussen, inklusive replikation og transskription, og pakning og beskytte -
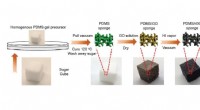 Strækbare natriumionbatterielektroder fremstillet ved hjælp af sukkerterningerEn sukkerterning fungerer som en skabelon for nye strækbare, svampeagtig, grafenbaserede batterielektroder. Kredit:Li et al. © 2017 WILEY-VCH (Phys.org) —Forskere har brugt sukkerterninger som en
Strækbare natriumionbatterielektroder fremstillet ved hjælp af sukkerterningerEn sukkerterning fungerer som en skabelon for nye strækbare, svampeagtig, grafenbaserede batterielektroder. Kredit:Li et al. © 2017 WILEY-VCH (Phys.org) —Forskere har brugt sukkerterninger som en
- Hvilket udtryk beskriver strukturen direkte under væv i hierarkisk organisering af livet?
- Lamborghini har allerede solgt alle sine biler indtil 2024
- Gravitationsbølgedetektorer til at søge efter mørkt stof
- Hvad ville der ske med solpaneler, hvis der ikke var sol ude?
- Har du en gammel iPhone? Det understøtter muligvis ikke iOS 15, og du vil gå glip af disse funktio…
- Fysikeres algoritme forudsiger molekylers optiske egenskaber


