Forståelse af polaritet i kemi:Hvordan elektroner former molekyler
Emilija Randjelovic/iStock/GettyImages
Elektroner i en kemisk binding
Når atomer samles, deler de elektroner, der danner en sky omkring kernerne. I kovalente bindinger deles elektrontætheden ligeligt, men i polære bindinger trækkes elektronerne mod det mere elektronegative atom, hvilket skaber en let ladningsubalance.
Bestemmelse af polaritet
Polaritet afhænger af elektronegativitet, det træk, som hvert atom udøver på delte elektroner. Beregn elektronegativitetsforskellen:
- 0,4–1,7→polær kovalent binding
- >1,7→ionisk karakter (elektroner overføres til det mere elektronegative atom)
- <0.4→ikke-polær kovalent binding (lige deling)
Dipolmoment
Polære bindinger genererer et dipolmoment:en negativ partiel ladning på det mere elektronegative atom og en positiv partiel ladning på den anden. Vektorsummen af alle bindingsdipoler giver molekylets netto dipolmoment, hvilket påvirker egenskaber såsom vands høje overfladespænding.
Polære vs. ikke-polære molekyler
Et molekyle kan indeholde polære bindinger og alligevel være generelt upolært, hvis dipolerne ophæver. For eksempel har CO₂ to polære C–O-bindinger (forskel 1,0), men den lineære geometri gør de to dipoler lige store og modsatte, hvilket giver et upolært molekyle.
Sidste artikelBeregning af ΔH:En praktisk guide til entalpiændringer
Næste artikelSådan afgøres, om et stof er surt:En praktisk vejledning
 Varme artikler
Varme artikler
-
 En ny teknik til at producere billigere og mere effektiv klorFigur 1:Karakterisering af Pt1/CNT-katalysator omfattende atomisk dispergerede Pt?N4-steder på overfladen af CNT. Kredit:UNIST Klor er et af de mest udbredte industrielle kemikalier i verden i d
En ny teknik til at producere billigere og mere effektiv klorFigur 1:Karakterisering af Pt1/CNT-katalysator omfattende atomisk dispergerede Pt?N4-steder på overfladen af CNT. Kredit:UNIST Klor er et af de mest udbredte industrielle kemikalier i verden i d -
 Udrugbare sygdomme får et nyt værktøj til opdagelse af RNA-lægemidlerScripps forskningskemiker Matthew Disney, PhD, og kandidatstuderende Blessy Suresh i deres Jupiter, Florida laboratorium. Kredit:Scripps Research Forestil dig, at du prøver at kaste et blik, når d
Udrugbare sygdomme får et nyt værktøj til opdagelse af RNA-lægemidlerScripps forskningskemiker Matthew Disney, PhD, og kandidatstuderende Blessy Suresh i deres Jupiter, Florida laboratorium. Kredit:Scripps Research Forestil dig, at du prøver at kaste et blik, når d -
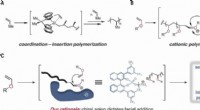 Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition
Brug af en organokatalysator til at stereokontrollere polymerisationDesign af en stereoselektiv kationisk polymerisation. (A) Det chirale ligandmiljø i koordinations-insertion-polymerisationer muliggør stereoselektiv monomer-enchainment ved at dirigere ansigtsaddition -
 Fem grundlæggende egenskaber ved gasserAf W.D. Johnson Opdateret 24. marts 2022 Eliza Snow/iStock/Getty Images Gasser var en gåde for tidlige videnskabsmænd, forbløffet over deres bevægelsesfrihed og tilsyneladende vægtløshed sammenligne
Fem grundlæggende egenskaber ved gasserAf W.D. Johnson Opdateret 24. marts 2022 Eliza Snow/iStock/Getty Images Gasser var en gåde for tidlige videnskabsmænd, forbløffet over deres bevægelsesfrihed og tilsyneladende vægtløshed sammenligne
- Hvilken direkte drejer jorden?
- Polen giver giftige alger skylden for at dræbe fisk i Oder-floden
- Hvilken type enhed inkluderer en hvilken som helst punktkilde, der udsender stråling uden aktivt at…
- Hvad ville der ske, hvis en organisme manglede hexokinase?
- Indvirkningen af veje og jernbaner på urbaniseringen aftager
- Linnéklassificering: Definition, niveauer og eksempler (med kort)


