Natriumbicarbonat:Fysiske og kemiske egenskaber forklaret
Af A.P. Mentzer | Opdateret 30. august 2022
eskaylim/iStock/GettyImages
Bagepulver, kemisk kendt som natriumbicarbonat (NaHCO₃), er en daglig basis og en alsidig forbindelse i videnskabelige laboratorier. Dens målbare fysiske og kemiske egenskaber gør den til et lærebogseksempel på, hvordan stof opfører sig under forskellige forhold.
Molekylær sammensætning
Natriumbicarbonat består af et natrium (Na), et kulstof (C), et hydrogen (H) og tre oxygen (O) atomer, hvilket giver det formlen NaHCO3 eller CHNaO3. Efter vægt er forbindelsen 57,1% natrium, 27,4% oxygen, 14,3% kulstof og 1,2% hydrogen.
jordachelr/iStock/Getty Images
Observerede fysiske egenskaber
Stoffet fremstår som et hvidt, krystallinsk pulver, der nogle gange klumper sig til små klumper. Den er lugtfri og giver en mildt bitter, salt smag. Ved stuetemperatur er natriumbicarbonat et fast stof. Dets opløselighed er en vigtig fysisk egenskab:det opløses let i vand og kan genvindes ved simpel fordampning.
eskaylim/iStock/Getty Images
Kemiske egenskaber
Nøgle kemiske adfærd omfatter dens alkalinitet og termisk nedbrydning. En 1% molær opløsning af bagepulver i vand har en pH på 8,3, hvilket placerer den fast i det alkaliske område og forklarer dens bitre smag. Når det opvarmes til over 50°C (122°F), nedbrydes natriumbicarbonat til kuldioxid (CO₂), vand (H₂O) og en lille mængde natriumcarbonat (Na₂CO₃), en proces, der frigiver gas og bruges til hæveapplikationer.
Brooke Fuller/iStock/Getty Images
Praktiske applikationer
Bagepulverets alkaliske natur gør det muligt for den at neutralisere syrer, hvilket gør den effektiv til rengøring, deodorisering og bagning. Dens milde slibeevne gør den også velegnet til skånsom skrubning, såsom at rense tænder eller fjerne pletter fra overflader.
sugar0607/iStock/Getty Images
MITSUHARU MAEDA/a.collectionRF/amana images/Getty Images
Sidste artikelFem nøgleindikatorer for, at der sker en kemisk reaktion
Næste artikelMateriens tre tilstande forklaret for børn
 Varme artikler
Varme artikler
-
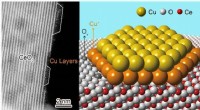 Forskere identificerer atomstruktur af katalytisk aktiv kobber-ceria-grænsefladeAtomstruktur af kobber-ceria-grænsefladen Kredit:DICP For nylig, Dr. Zhou Yan og prof. Shen Wenjie ved Dalian Institute of Chemical Physics (DICP) fra det kinesiske videnskabsakademi og deres sama
Forskere identificerer atomstruktur af katalytisk aktiv kobber-ceria-grænsefladeAtomstruktur af kobber-ceria-grænsefladen Kredit:DICP For nylig, Dr. Zhou Yan og prof. Shen Wenjie ved Dalian Institute of Chemical Physics (DICP) fra det kinesiske videnskabsakademi og deres sama -
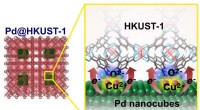 Grænseflade elektronisk tilstand, der forbedrer brintlagringskapacitet i Pd-MOF-materialer(Venstre) Struktur af en Pd@HKUST-1. (Højre) Skematisk diagram, der illustrerer overførslen af elektrisk ladning fra en Pd nanocube til HKUST-1 MOFer (metal-organiske rammer) Kredit:NIMS NIMS, K
Grænseflade elektronisk tilstand, der forbedrer brintlagringskapacitet i Pd-MOF-materialer(Venstre) Struktur af en Pd@HKUST-1. (Højre) Skematisk diagram, der illustrerer overførslen af elektrisk ladning fra en Pd nanocube til HKUST-1 MOFer (metal-organiske rammer) Kredit:NIMS NIMS, K -
 Brygget kaffegrums tilbyder et bæredygtigt alternativ til farvestof til tøjKredit:Iowa State University Forskere fra Iowa State University har fundet en naturlig måde at tilføje farve til tøjet ved at bruge resterne fra din daglige kop kaffe. Tekstilindustrien bruger me
Brygget kaffegrums tilbyder et bæredygtigt alternativ til farvestof til tøjKredit:Iowa State University Forskere fra Iowa State University har fundet en naturlig måde at tilføje farve til tøjet ved at bruge resterne fra din daglige kop kaffe. Tekstilindustrien bruger me -
 Gennemstrømningselektroder gør brint 50 gange hurtigereEt eksempel på de små, gennemstrømningselektrode, som Duke-forskere brugte til at producere mere brint fra elektrolyse med en krone til skala. Kredit:Wiley Lab, Duke University Elektrolyse, passer
Gennemstrømningselektroder gør brint 50 gange hurtigereEt eksempel på de små, gennemstrømningselektrode, som Duke-forskere brugte til at producere mere brint fra elektrolyse med en krone til skala. Kredit:Wiley Lab, Duke University Elektrolyse, passer
- OS, Russisk, Japanske astronauter vender tilbage fra ISS
- Hvordan kæmpe tang kan reagere på klimaændringer
- COVID-19 antistoftest:Hvor pålidelige er de?
- Hvad er 94,1f i Kelvin?
- Hvordan kan jeg sikkert se solformørkelsen ved hjælp af svejsningsbriller?
- Det voksende energibehov for fritidsrejser senere i livet


