Hvilke produkter dannes, når man blander en syre med en base? En detaljeret guide til neutralisering
Forståelse af kemien ved syre-base-blanding
En neutraliseringsreaktion - blanding af en syre med en base - producerer altid nye kemikalier fra de oprindelige reaktanter. De specifikke produkter afhænger af identiteten af syren, basen og den støkiometriske balance mellem dem. Nedenfor er en klar, autoritativ forklaring på, hvad man kan forvente, fra klassiske stærk-syre/stærk-base-systemer til mere komplekse svag-syre/svag-base og gasdannende reaktioner.
Typisk stærk syre og stærke basereaktioner
I en opløsning af vand kombineres en stærk syre (fuldstændig dissocieret) og en stærk base (fuldstændig dissocieret) for at danne vand og et salt. Det klassiske eksempel er saltsyre og natriumhydroxid:
HCl + NaOH → H2O + NaCl
Her forbliver NaCl (bordsalt) opløst som ioner i det vandige medium.
Detaljeret eksempel:Salpetersyre og kaliumhydroxid
Blanding af den stærke sure salpetersyre (HNO₃) med den stærke base kaliumhydroxid (KOH) giver:
HNO3 + KOH → H2O + KNO3
Produktet, kaliumnitrat (KNO₃), er et salt, der dissocieres til K⁺- og NO₃⁻-ioner i vand.
Fuldstændig ionisk ligning
For at visualisere dissociation skriver kemikere en komplet ionisk ligning:
H+(aq) + NO3⁻(aq) + K⁺(aq) + OH⁻(aq) → H2O(l) + K⁺(aq) + NO3⁻(aq)
Dette viser, at syren og basen er fuldt ioniseret, og den eneste kemiske ændring er dannelsen af vand.
Net-ionisk ligning
Fjernelse af tilskuerioner giver den nettoioniske ligning:
H⁺(vandig) + OH⁻(vandig) → H2O(l)
Dette indikerer, at den sande reaktion er neutraliseringen af H+ og OH⁻ til dannelse af vand; K⁺- og NO3⁻-ionerne forbliver uændrede.
Stykiometri:Sikring af fuldstændig neutralisering
For at opnå en ren produktblanding (salt + vand) skal det støkiometriske forhold mellem syre og base være nøjagtigt. Overskydende syre efterlader resterende H⁺ i opløsningen; overskydende base efterlader resterende OH⁻. Beregning af de nødvendige mængder er et standard støkiometriproblem, der findes i de fleste kemipensum.
Svage syrer, svage baser og yderligere produkter
Når en af reaktanterne er svage, fortsætter reaktionen stadig, men med forskellig ioniseringsadfærd. For eksempel giver blanding af natriumbicarbonat (NaHCO₃) med en svag eller stærk syre ofte en gas:
HCl + NaHCO3 → NaCl + H2O + CO2(g)
Her frigives kuldioxid, så produkterne indeholder en gas udover salt og vand.
Vigtige ting
- Stærk syre + stærk base → vand + salt.
- Svage syrer/baser kan ændre omfanget af ionisering.
- Overskydende reaktant forbliver i den endelige blanding, hvis støkiometri er slået fra.
- Syre-bicarbonat-reaktioner kan producere CO₂-gas.
For et dybere dyk, se standardreferencer såsom Atkins &de Paula, Fysisk kemi eller Marion &H. E. Mason, Chemistry:A Molecular Approach .
 Varme artikler
Varme artikler
-
 Inside the Ink:The Science Behind Ballpoint PensAf Blake Flournoy | Opdateret 30. august 2022 Sky_Blue/iStock/GettyImages Fra et lædergarveri til det moderne skrivebord Mens den første kuglepen dukkede op i 1888, tog det næsten seks årtiers forfi
Inside the Ink:The Science Behind Ballpoint PensAf Blake Flournoy | Opdateret 30. august 2022 Sky_Blue/iStock/GettyImages Fra et lædergarveri til det moderne skrivebord Mens den første kuglepen dukkede op i 1888, tog det næsten seks årtiers forfi -
 Solens UV-lys hjalp med at tænde livMens mange undersøgelser er fokuseret på de skadelige virkninger af højenergi UV-sollys, det er også en vigtig energikilde, der kan drive dannelsen af biomolekyler, der er relevante for livet. Kredi
Solens UV-lys hjalp med at tænde livMens mange undersøgelser er fokuseret på de skadelige virkninger af højenergi UV-sollys, det er også en vigtig energikilde, der kan drive dannelsen af biomolekyler, der er relevante for livet. Kredi -
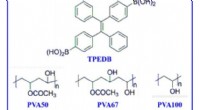 Storskala fremstilling af polymerbaseret stuetemperatur phosphorescens via klikkemiMolekylformler for fosfor og polymermatricer. De molekylære formler for TPEDB, PVA med forskellig alkohollysegrad (PVA50, PVA67, PVA100), og kontrollerede polymerer (PDDA, PSS, og PVDF). Kredit:Scienc
Storskala fremstilling af polymerbaseret stuetemperatur phosphorescens via klikkemiMolekylformler for fosfor og polymermatricer. De molekylære formler for TPEDB, PVA med forskellig alkohollysegrad (PVA50, PVA67, PVA100), og kontrollerede polymerer (PDDA, PSS, og PVDF). Kredit:Scienc -
 Skræddersyede enzymatiske løsninger reducerer tid og omkostninger ved bioraffinaderierKredit:MetGen Ikke mad, træagtige materialer (nemlig lignocelluloseholdig biomasse) er det største vedvarende reservoir af fermenterbar stivelse til erstatning for fossile brændstoffer. Det kan br
Skræddersyede enzymatiske løsninger reducerer tid og omkostninger ved bioraffinaderierKredit:MetGen Ikke mad, træagtige materialer (nemlig lignocelluloseholdig biomasse) er det største vedvarende reservoir af fermenterbar stivelse til erstatning for fossile brændstoffer. Det kan br
- Hvad måler en GPS i jordskælv?
- Sådan beregnes terningssandsynligheder
- Hvad er de biotiske og abiotiske egenskaber ved tropisk regnskov?
- Mikrobiel biomasseændring ændrer jernoxidernes rolle i organisk C-mineralisering i anoxisk uafskal…
- Brint:Nøgleegenskaber og fakta om universets mest rigelige grundstof
- Energi, der er opbevaret på grund af position eller form kaldet hvad?


