Forståelse af Lewis-syrer:definition, eksempler og katalytisk rolle
AndreaObzerova/iStock/GettyImages
Syrer og baser er velkendte begreber i kemi, men udtrykket Lewis-syre refererer til en særskilt klasse af reaktanter. Mens Brønsted–Lowry-rammen fokuserer på protonoverførsel, har G.N. Lewis udvidede definitionen til at omfatte enhver reaktion, hvor elektronpar udveksles, og derved inkluderede ikke-protoniske processer.
TL;DR
Lewis-syrer accepterer elektronpar, hvorimod Lewis-baser donerer dem. En elektron-deficient eller positivt ladet art fungerer typisk som en Lewis-syre.
I 1923 demonstrerede Lewis dette princip ved at bruge en hydrogenion (H⁺) og hydroxidionen (OH⁻). Mens Brønsted-Lowry-teorien beskriver, at OH⁻ accepterer en proton for at danne vand, så Lewis hydrogenionen som en elektronacceptor, der danner en kovalent binding med elektronparret fra hydroxid.
Definition af en Lewis-syre
En Lewis-syre er enhver kemisk art, der er i stand til at danne en kovalent binding ved at acceptere et elektronpar fra en anden art. Disse syrer har ofte ledige orbitaler, der kan rumme de indkommende elektroner.
Omvendt en Lewis-base er en art, der donerer et elektronpar for at danne en kovalent binding. Forholdet mellem Lewis-syrer og baser er analogt med den klassiske syre-base-parring, men er defineret ved elektronparoverførsel snarere end protonoverførsel.
Eksempler på Lewis-syrer omfatter metalkationer såsom Al³⁺ og Fe³⁺, hvis positive ladning stærkt tiltrækker elektrontæthed.
Lewis-syrekatalysatorer
En Lewis-syrekatalysator accelererer en kemisk reaktion ved at acceptere elektroner fra et substrat og derved øge dens reaktivitet. Det er vigtigt, at selve katalysatoren ikke forbruges i reaktionen; det regenereres i slutningen af den katalytiske cyklus.
AlCl3 som en Lewis-syre
AlCl3 er en lærebog Lewis-syre. Aluminium har 17 valenselektroner, hvilket efterlader en tom p-orbital, der kan acceptere et elektronpar. Denne elektron-accepterende evne gør det muligt for AlCl₃ at lette adskillige organiske transformationer.
NH₃ (ammoniak) som en Lewis-base
Ammoniak indeholder et ensomt par elektroner på nitrogen, hvilket gør det muligt for det at donere dette par til en elektron-accepterende art. Når NH₃ reagerer med HCl i vandig opløsning, donerer nitrogenet elektroner til H⁺ og danner NH₄⁺.
Både Brønsted-Lowry- og Lewis-koncepterne beskriver relateret kemisk adfærd, men fra forskellige perspektiver - protonoverførsel versus elektronparoverførsel. Forståelse af begge rammer giver et omfattende overblik over syre-base kemi.
 Varme artikler
Varme artikler
-
 Brug af lignin til at erstatte fossile materialerForskningen og udnyttelsen af kuglelignende ligninpartikler er stadig ny, men produktionen er allerede mulig i partier på flere kilo. Det gør det muligt at teste dem i forskellige applikationer, sig
Brug af lignin til at erstatte fossile materialerForskningen og udnyttelsen af kuglelignende ligninpartikler er stadig ny, men produktionen er allerede mulig i partier på flere kilo. Det gør det muligt at teste dem i forskellige applikationer, sig -
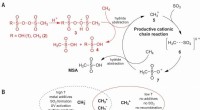 Methanoxidation på plussiden – En selektiv industriel vej til methansulfonsyre(A) Foreslået ionisk reaktionsmekanisme til CH-aktivering af CH4 i den selektive produktion af MSA (methansulfonsyre). (B) Fordele ved den kationiske vej frem for den radikale vej. T, temperatur. Kred
Methanoxidation på plussiden – En selektiv industriel vej til methansulfonsyre(A) Foreslået ionisk reaktionsmekanisme til CH-aktivering af CH4 i den selektive produktion af MSA (methansulfonsyre). (B) Fordele ved den kationiske vej frem for den radikale vej. T, temperatur. Kred -
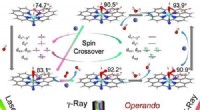 Forskere identificerer elektroniske og strukturelle dynamikker i katalytiske centre i enkelt-Fe-atom…Identifikationen af den elektroniske og strukturelle dynamik af katalytiske centre i enkelt-Fe-atom materiale ved Operando Mossbauer spektroskopi. Kredit:LI Xuning Single-atom catalyst (SAC) er
Forskere identificerer elektroniske og strukturelle dynamikker i katalytiske centre i enkelt-Fe-atom…Identifikationen af den elektroniske og strukturelle dynamik af katalytiske centre i enkelt-Fe-atom materiale ved Operando Mossbauer spektroskopi. Kredit:LI Xuning Single-atom catalyst (SAC) er -
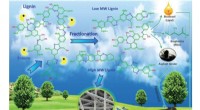 Bjerge af affald kan føre til ny amerikansk fremstilling, jobEt affaldsmateriale fra papir- og papirmasseindustrien kunne snart laves til alt fra tennisketcher til biler, ifølge nye fund fra Texas A&M AgriLife Research -forskere. Kredit:Texas A&M AgriLife Resea
Bjerge af affald kan føre til ny amerikansk fremstilling, jobEt affaldsmateriale fra papir- og papirmasseindustrien kunne snart laves til alt fra tennisketcher til biler, ifølge nye fund fra Texas A&M AgriLife Research -forskere. Kredit:Texas A&M AgriLife Resea
- Beskriv den indre kerne af jorden?
- Er der en konstellation, der består af 3 lyse stjerner i række den østlige himmel?
- Beskytter det at være en 'superwoman' afroamerikanske kvinders sundhed?
- Hvad er den fysiske beskrivelse af Mars?
- Hvilke agenter medfører kemisk forvitring på klipper A.Rainwater B.Ocean vand C.Flowing D. Alle af…
- Afrikas fødevareorganisation lever ikke op til løftet om at fordoble udbyttet


