Sådan beregnes den empiriske formel:En trin-for-trin guide
pattonmania/iStock/GettyImages
Den empiriske formel repræsenterer det enkleste hele-talsforhold mellem atomer i et molekyle. Selvom det ikke afslører det nøjagtige antal eller arrangement af atomer, er det uundværligt for støkiometri, den analytiske gren, der undersøger reaktant- og produktsammensætninger i kemiske reaktioner. Nedenfor er en kortfattet gennemgang på ekspertniveau til at bestemme den empiriske formel ud fra grundstofmasserne af en prøve.
TL;DR
Empiriske formler giver de relative andele af hvert grundstof i en forbindelse, ikke det absolutte antal eller struktur.
1. Bestem massen af hvert element
Start med prøvens grundstofmasser. For eksempel:13,5 g Ca, 10,8 g O og 0,675 g H.
2. Hent atomvægte
Se IUPAC's periodiske tabel for atomvægte:Ca=40,1g/mol, O=16,0g/mol, H=1,01g/mol.
3. Konverter masser til mol
- Ca:13,5 g ÷ 40,1 g/mol=0,337 mol
- O:10,8 g ÷ 16,0 g/mol=0,675 mol
- H:0,675 g ÷ 1,01 g/mol=0,668 mol
4. Etabler Elemental Ratio
Divider hver molværdi med den mindste (Ca, 0,337mol):
- Ca:0,337 ÷ 0,337=1
- O:0,675 ÷ 0,337≈2
- H:0,668 ÷ 0,337≈2
5. Skriv den empiriske formel
Kombiner forholdene for at opnå den enkleste formel:CaO₂H₂ . Dette angiver et Ca-atom for hver to O- og to H-atomer i den enkleste repræsentation.
Husk, den empiriske formel er et grundlæggende værktøj til støkiometriske beregninger, der gør det muligt for kemikere at forudsige reaktionsresultater og syntetisere forbindelser med præcision.
Sidste artikelHvordan syrer og baser former vores hverdag
Næste artikelSådan beregnes ΔHf:En praktisk guide til dannelsens standardentalpi
 Varme artikler
Varme artikler
-
 Lab afslører hjerte-på-en-chipGennem hjerte-på-en-chip-teknologi - modellering af et menneskeligt hjerte på en konstrueret chip og måling af virkningerne af forbindelseseksponering ved hjælp af mikroelektroder - håber Lawrence Liv
Lab afslører hjerte-på-en-chipGennem hjerte-på-en-chip-teknologi - modellering af et menneskeligt hjerte på en konstrueret chip og måling af virkningerne af forbindelseseksponering ved hjælp af mikroelektroder - håber Lawrence Liv -
 Tænd og sluk for en porøs materialefarve med syreBillede af den skabte hydrogenbinding organiske ramme CPHATN- (TCB) (til venstre), og dens aktiverede version, CPHATN-1a (højre). Kredit:Hisaki I. et al., Syreresponsive, hydrogenbundne organiske ramm
Tænd og sluk for en porøs materialefarve med syreBillede af den skabte hydrogenbinding organiske ramme CPHATN- (TCB) (til venstre), og dens aktiverede version, CPHATN-1a (højre). Kredit:Hisaki I. et al., Syreresponsive, hydrogenbundne organiske ramm -
 Sådan testes en modstandstemperaturdetektor (RTD) for nøjagtig ydeevneAf Jill Kokemuller, Opdateret 24. marts 2022 Hemera Technologies/AbleStock.com/Getty Images Resistance Temperature Detectors (RTDer) er afhængige af den forudsigelige ændring i et metals resistivite
Sådan testes en modstandstemperaturdetektor (RTD) for nøjagtig ydeevneAf Jill Kokemuller, Opdateret 24. marts 2022 Hemera Technologies/AbleStock.com/Getty Images Resistance Temperature Detectors (RTDer) er afhængige af den forudsigelige ændring i et metals resistivite -
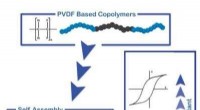 Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam
Ferroelektriske polymerer gjort mere alsidigeEn blokcopolymer af PVDF (sort) og en isolerende polymerkæde (blå) danner en blokcopolymer. Gennem faseadskillelse, blokkene samles i film. De dielektriske egenskaber kan indstilles ved at variere sam
- Hvor mange hydrogenatomer er på venstre side af fotosyntese ligning?
- Metasurface løser beregningsproblemer som en analog computer
- Hvordan produceres og diliveres termisk energi til dig gennem et fladt jern?
- Hvad er en energiændring?
- Hvem er skytshelgen for meteorologi?
- Hvordan tjener parringen af baser som et mønster eller kode til fremstilling af nøjagtige kromos…


