Molaritet Forklaret:Definition, beregning og praktiske eksempler
Af Michael Merry
Opdateret 30. august 2022
Hinterhaus Productions/DigitalVision/GettyImages
Forståelse af koncentration i kemi
I kemisk arbejde er det vigtigt at vide, hvor meget af et stof der er opløst i en given mængde opløsning. Denne måling er kendt som koncentration, og molaritet er den mest udbredte enhed til at udtrykke den. Molaritet stemmer perfekt overens med støkiometriske beregninger, fordi reaktanter kombineres i hele tal-molforhold. For eksempel involverer reaktionen 2H2 + O2 → 2H2O 2 mol hydrogengas, der reagerer med 1 mol oxygengas for at give 2 mol vand.
Muldvarpen:En tælleenhed for atomer og molekyler
Et mol er defineret som mængden af et stof, der indeholder nøjagtigt 6,022×10²³ elementære enheder – atomer, molekyler, ioner eller andre partikler. Denne værdi, kendt som Avogadros tal, blev aftalt internationalt baseret på antallet af atomer i 12g af kulstof-12-isotopen. Brug af denne tælleenhed forenkler masseberegninger:1 mol ilt vejer 16,00 g, 1 mol vand 18,02 g og 1 mol kuldioxid 44,01 g.
Hvad er molaritet?
Molaritet, angivet med symbolet M, er antallet af mol af et opløst stof opløst i en liter opløsning. Det adskiller sig fra molalitet, som udtrykker mol opløst stof pr. kilogram opløsningsmiddel. Molaritet foretrækkes i laboratoriemiljøer, fordi den er direkte relateret til mængden af opløsning, der bruges i reaktioner.
Beregning af molaritet:Et trin-for-trin-eksempel
Antag, at du har brug for molariteten af en opløsning, der indeholder 100 g natriumchlorid (NaCl) i 2,5 l opløsning.
Trin 1:Bestem formelvægten af NaCl.
Na (22,99 g/mol) + Cl (35,45 g/mol) =58,44 g/mol.
Trin 2:Find antallet af mol NaCl.
100 g ÷ 58,44 g/mol =1,71 mol.
Trin 3:Beregn molaritet.
1,71 mol ÷ 2,5 L =0,684 M.
Forberedelse af en løsning af en ønsket molaritet
Hvor meget natriumsulfat (Na₂SO4) skal der til for at lave 250 ml af en 0,5 M opløsning?
Trin 1:Beregn påkrævede mol.
0,25L × 0,5mol/L =0,125mol.
Trin 2:Beregn formelvægten af Na₂SO4.
2Na (22,99 g/mol × 2) + S (32,07 g/mol) + 4O (16,00 g/mol × 4) =142,1 g/mol.
Trin 3:Bestem massen af Na₂SO₄.
0,125 mol × 142,1 g/mol =17,76 g.
Disse ligefremme beregninger illustrerer, hvordan molaritet muliggør præcis fremstilling og analyse af kemiske opløsninger.
 Varme artikler
Varme artikler
-
 Kold sintring producerer kondensatormateriale ved rekordlave temperaturerDen tætte mikrostruktur af bariumtitanat set under et mikroskop. Kredit:Pennsylvania State University Bariumtitanat er et vigtigt elektrokeramisk materiale, der bruges i billioner af kondensatorer
Kold sintring producerer kondensatormateriale ved rekordlave temperaturerDen tætte mikrostruktur af bariumtitanat set under et mikroskop. Kredit:Pennsylvania State University Bariumtitanat er et vigtigt elektrokeramisk materiale, der bruges i billioner af kondensatorer -
 På linjen:At se nanopartikler komme i formKredit:Lawrence Berkeley National Laboratory Flydende strukturer - flydende dråber, der bevarer en bestemt form - er nyttige til en række forskellige anvendelser, fra fødevareforarbejdning til kos
På linjen:At se nanopartikler komme i formKredit:Lawrence Berkeley National Laboratory Flydende strukturer - flydende dråber, der bevarer en bestemt form - er nyttige til en række forskellige anvendelser, fra fødevareforarbejdning til kos -
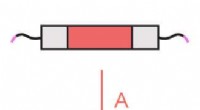 Forskere programmerer biomaterialer med logiske porte, der frigiver terapeutika som reaktion på mil…Repræsentation af en simpel JA port. De grå og orange søjler repræsenterer hele porten, som forbinder til polymererne, der holder hydrogel sammen (sorte og lilla bølgede linjer). Porten åbnes - frigiv
Forskere programmerer biomaterialer med logiske porte, der frigiver terapeutika som reaktion på mil…Repræsentation af en simpel JA port. De grå og orange søjler repræsenterer hele porten, som forbinder til polymererne, der holder hydrogel sammen (sorte og lilla bølgede linjer). Porten åbnes - frigiv -
 Chemputer lover app-styret revolution for lægemiddelproduktionEt billede af en kemputerobot. Kredit:Cronin Group, Kemiskolen, Glasgow En radikal ny metode til fremstilling af lægemiddelmolekyler, som bruger blueprints, der kan downloades, til let og pålideli
Chemputer lover app-styret revolution for lægemiddelproduktionEt billede af en kemputerobot. Kredit:Cronin Group, Kemiskolen, Glasgow En radikal ny metode til fremstilling af lægemiddelmolekyler, som bruger blueprints, der kan downloades, til let og pålideli
- Hvad giver energien til produktion af elektromagnetiske bølger i solen?
- Hvordan er cellulære strukturer involveret i syntese og emballageprotein?
- An-arrgh-chy! Hvad Blackbeard kan lære os om politik
- I et anlæg forklarer trykstrømshypotesen bevægelse af sukker fra til?
- Når solens stråler rammer jorden lavere vinkler og lyset spreder sig ud over større områder?
- Hvilket kropssystem regulerer aktiviteter gennem nerveimpulser?


