Sådan bestemmes et molekyles steriske nummer:En praktisk vejledning for kemikere
Af Lee Johnson – Opdateret 30. august 2022
Hvorfor steriske tal betyder noget
Geometrien af et molekyle er styret af frastødningen mellem elektronpar omkring dets centrale atom. Det steriske tal — summen af bundne atomer og enlige elektronpar — giver en hurtig og pålidelig måde at forudsige den form på.
Hvad er et sterisk tal?
Det er det samlede antal af:
- Atomer, der er direkte bundet til det centrale atom (hver binding, uanset enkelt, dobbelt eller tredobbelt, tæller som én)
- Ensomme elektrongrupper på det atom
Disse elektrongrupper arrangerer sig selv for at minimere frastødning, hvilket giver anledning til de velkendte VSEPR-former:
| Sterisk tal | Geometri |
|---|---|
| 2 | Lineær |
| 3 | Trigonal plan |
| 4 | Tetraedral |
| 5 | Trigonal bipyramidal |
| 6 | Oktaedral |
Udledning af det steriske tal fra en Lewis-struktur
1. Tegn Lewis-strukturen. Placer det centrale atom og forbind det til de omgivende atomer med det korrekte antal bindinger, ved at bruge molekylformlen som en guide.
2. Tæl obligationer. Hver binding til det centrale atom tilføjer en til totalen, selvom det er en dobbelt- eller tredobbeltbinding.
3. Identificer enlige par. Alle prikker eller elektronpar, der ikke er involveret i binding omkring det centrale atom, bidrager med én pr. par.
4. Anvend formlen.
Sterisk tal =(antal bundne atomer) + (antal enlige par)
Eksempel:Vand (H2 O)
Lewis-strukturen viser oxygen bundet til to hydrogenatomer. Ilt har seks valenselektroner; to bruges i O–H-bindingerne, hvilket efterlader fire som to ensomme par.
Beregner:
steric number = 2 (bonds) + 2 (lone pairs) = 4
Et sterisk tal på fire forudsiger et tetraedrisk elektron-par arrangement. I vand er to af disse positioner optaget af ensomme par, hvilket giver den observerede bøjede molekylære form.
Vigtige ting
- Dobbelt- og tredobbeltbindinger tæller som én, når det steriske tal bestemmes.
- Kun ensomme par på det centrale atom tages i betragtning – enlige par på perifere atomer påvirker ikke tællingen.
- Når du kan tegne en Lewis-struktur, er det steriske tal næsten øjeblikkeligt at beregne.
 Varme artikler
Varme artikler
-
 Sådan opløses papir sikkert med muriatinsyre (saltsyre).Af Jason Williams – Opdateret 24. marts 2022 Papir er overraskende modstandsdygtigt over for almindelige opløsningsmidler. De fleste kommercielle papirer har en næsten neutral pH, så en stærk syre så
Sådan opløses papir sikkert med muriatinsyre (saltsyre).Af Jason Williams – Opdateret 24. marts 2022 Papir er overraskende modstandsdygtigt over for almindelige opløsningsmidler. De fleste kommercielle papirer har en næsten neutral pH, så en stærk syre så -
 Forståelse af forbrændingsreaktioner:Hvordan ild omdanner brændstof til energiEn forbrændingsreaktion, ofte forkortet RXN, er den kemiske proces, hvor et brændbart stof reagerer med ilt og frigiver varme og lys. Mens mange reaktioner producerer varme, deler ægte forbrændingsre
Forståelse af forbrændingsreaktioner:Hvordan ild omdanner brændstof til energiEn forbrændingsreaktion, ofte forkortet RXN, er den kemiske proces, hvor et brændbart stof reagerer med ilt og frigiver varme og lys. Mens mange reaktioner producerer varme, deler ægte forbrændingsre -
 Ingeniørers reaktor omdanner gas direkte til eddikesyreEt elektronmikroskop viser billeder af kobber -nanokuber, der blev brugt af ingeniører fra Rice University til at katalysere omdannelsen af kulilte til eddikesyre. Kredit:Wang Group/Senftle Group/Ri
Ingeniørers reaktor omdanner gas direkte til eddikesyreEt elektronmikroskop viser billeder af kobber -nanokuber, der blev brugt af ingeniører fra Rice University til at katalysere omdannelsen af kulilte til eddikesyre. Kredit:Wang Group/Senftle Group/Ri -
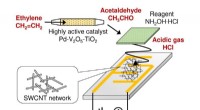 Udvikling af en lille sensor, der er i stand til løbende at overvåge phytohormon ethylenEn lille, meget følsom sensor, der er i stand til at detektere ethylen med stor selektivitet. Kredit:NIMS NIMS og AIST har udviklet en lille sensor, der er i stand til kontinuerligt at overvåge pl
Udvikling af en lille sensor, der er i stand til løbende at overvåge phytohormon ethylenEn lille, meget følsom sensor, der er i stand til at detektere ethylen med stor selektivitet. Kredit:NIMS NIMS og AIST har udviklet en lille sensor, der er i stand til kontinuerligt at overvåge pl
- Eksperimentel demonstration af måleafhængige realiteter mulig, siger forsker
- Hvad er K-Shell-bindende energi til Rhodium?
- Insekter kæmper for at tilpasse sig ekstreme temperaturer, hvilket gør dem sårbare over for klima…
- Hvilket fly skærer kroppen i øvre og nedre halvdele?
- Tidlige jæger-samlere interagerede meget hurtigere end tidligere antaget
- Hvor mange huse blev ødelagt, efter at Mt Vesuvius brød ud i 79 e.Kr.


