Beregning af hydroniumionkoncentration ud fra pH (og omvendt)
Af Tracy McConnell, Opdateret 30. august 2022
deyangeorgiev/iStock/GettyImages
pH-skalaen - fra 0 til 14 - kvantificerer surheden eller alkaliniteten af en opløsning. At forstå en opløsnings pH er afgørende i både undervisningsmiljøer og laboratoriepraksis, da det informerer os om de tilstedeværende arter og forudsiger, hvordan opløsningen vil opføre sig i kemiske reaktioner.
Fordi pH direkte afspejler koncentrationen af hydroniumioner (H₃O⁺) i vand, kan den bruges til at beregne koncentrationen af andre ioner i systemet. Følgende ligninger danner grundlaget for disse beregninger.
pH- og hydroniumkoncentration
Forholdet mellem pH og hydroniumionkoncentration er udtrykt som:
pH=−log10[H3O+]
Her angiver parenteserne molaritet. Når [H3O+] er kendt, kan pH bestemmes; omvendt tillader en målt pH beregning af [H₃O⁺].
Eksempel1:Bestem pH ud fra [H₃O⁺]
I en 1,0L prøve af 0,1M saltsyre (HCl) er hydroniumkoncentrationen 1×10⁻¹M.
pH=−log₁₀(1×10⁻¹)=−(−1)=1,00
Eksempel2:Bestem [H₃O⁺] ud fra pH
Hvis en opløsning har en pH på 4,3, giver omarrangering af pH-ligningen:
[H₃O⁺]=10^−pH=10^−4,3≈5,01×10⁻⁵M
Eksempel3:Basisberegninger ved hjælp af ionproduktet af vand
For basiske opløsninger er koncentrationen af hydroxidioner [OH⁻] lettere at måle. Ved at bruge ionproduktkonstanten for vand (K_w=1×10⁻¹⁴ ved 25°C), finder vi:
[H3O+]=K_w/[OH⁻]
Med [OH⁻]=4,0×10⁻¹¹M:
1. [H3O⁺]=(1×10⁻¹⁴) / (4,0×10⁻¹¹)=2,5×10⁻⁴M
2. pH=−log₁₀(2,5×10⁻⁴)≈3,60
Væsentlige tal i pH-beregninger
pH-værdier rapporteres typisk til nærmeste tiendedel eller hundrededel, hvilket afspejler målingens præcision. Når du anvender logaritmen, betragtes kun cifrene efter decimaltegnet som signifikante, hvilket sikrer overensstemmelse med eksperimentel usikkerhed.
Syredissociationskonstant (K_a)
Syredisssociationskonstanten kvantificerer, i hvilket omfang en syre ioniserer i vand. Svage syrer har små K_a-værdier, hvilket betyder, at det meste af syren forbliver udissocieret, hvorimod stærke syrer har store K_a-værdier og ioniserer næsten fuldstændigt.
Eksempel:Kulsyre (H₂CO₃) er en svag, diprotisk syre med
H₂CO₃(aq)⇌HCO₃⁻(aq)+H⁺(aq) K_a₁=4,3×10⁻⁷
og et andet dissociationstrin:
HCO₃⁻(aq)⇌CO₃²⁻(aq)+H⁺(aq) K_a₂=4,8×10⁻¹¹
I modsætning hertil er salpetersyre (HNO₃) en stærk syre med K_a≈40, hvilket illustrerer dens næsten fuldstændige dissociation.
 Varme artikler
Varme artikler
-
 Forskning viser Krebs cyklus mulig uden metaller eller enzymkatalysatorer, giver nye ledetråde til …Trent Stubbs 20 i laboratorium med Furman kemiprofessor Greg Springsteen. Kredit:Jeremy Fleming, Furman Universitet Nylig Furman University-kandidat Trent Stubbs er forfatter til en ny undersøgels
Forskning viser Krebs cyklus mulig uden metaller eller enzymkatalysatorer, giver nye ledetråde til …Trent Stubbs 20 i laboratorium med Furman kemiprofessor Greg Springsteen. Kredit:Jeremy Fleming, Furman Universitet Nylig Furman University-kandidat Trent Stubbs er forfatter til en ny undersøgels -
 Hvad WD-40 virkelig betyderHvad WD-40 virkelig betyder Ramzy Jalali/Shutterstock WD-40 har fået et ry som en alsidig dagligvare. Selvom det primært markedsføres som et smøremiddel, spænder det over rengøring, insektafskræknin
Hvad WD-40 virkelig betyderHvad WD-40 virkelig betyder Ramzy Jalali/Shutterstock WD-40 har fået et ry som en alsidig dagligvare. Selvom det primært markedsføres som et smøremiddel, spænder det over rengøring, insektafskræknin -
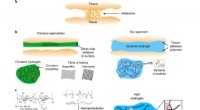 Forskere opdager, at gel reducerer arvæv efter operation hos dyren, Skematisk fremstilling af adhæsionsdannelse mellem to væv. b, Skematisk repræsentation af tidligere tilgange til at forhindre adhæsioner ved hjælp af solide adhæsionsbarrierer til fysisk at adskil
Forskere opdager, at gel reducerer arvæv efter operation hos dyren, Skematisk fremstilling af adhæsionsdannelse mellem to væv. b, Skematisk repræsentation af tidligere tilgange til at forhindre adhæsioner ved hjælp af solide adhæsionsbarrierer til fysisk at adskil -
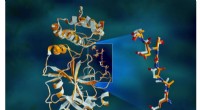 Røntgenstråler gør proteinstrukturen større i hjertet af COVID-19-virusOverlappende røntgendata for SARS-CoV-2-hovedproteasen viser strukturelle forskelle mellem proteinet ved stuetemperatur (orange) og den kryogenfrosne struktur (hvid). Kredit:Jill Hemman/ORNL, US Depar
Røntgenstråler gør proteinstrukturen større i hjertet af COVID-19-virusOverlappende røntgendata for SARS-CoV-2-hovedproteasen viser strukturelle forskelle mellem proteinet ved stuetemperatur (orange) og den kryogenfrosne struktur (hvid). Kredit:Jill Hemman/ORNL, US Depar
- Hvordan kvindelige hyæner kom til at dominere hannerne
- Hvilken måleenhed bruger længdegrad?
- Er det sandt eller falsk acceleration er størrelsen af den gennemsnitlige hastighed?
- Hvorfor producerer placering af to forskellige metaller i en frugt en elektrisk strøm?
- Hvad er relativitet?
- Latex Specifikationer og Egenskaber


